
Wetenschap
Waarom heeft zout water meer geleidbaarheid dan kraanwater?
* elektrolyten en geleidbaarheid: Geleidbaarheid in een oplossing wordt bepaald door zijn vermogen om elektriciteit te leiden. Dit vermogen is direct gerelateerd aan de aanwezigheid van vrij bewegende geladen deeltjes die ionen worden genoemd. Oplossingen die elektriciteit goed leiden, worden elektrolyten genoemd.
* Zoutdissociatie: Wanneer zout (natriumchloride, NaCl) oplost in water, dissocieert het in zijn samenstellende ionen:natriumionen (Na+) en chloride-ionen (Cl-). Deze ionen zijn vrij om door de oplossing te bewegen.
* Laad dragers: Deze vrij bewegende ionen fungeren als ladingsdragers, waardoor elektriciteit door de oplossing kan stromen. Hoe meer ionen aanwezig zijn, hoe beter de geleidbaarheid.
* kraanwater: Tandwater bevat een kleine hoeveelheid opgeloste mineralen, inclusief ionen, maar de concentratie is veel lager dan in zout water. Dit betekent dat leidingwater een lagere concentratie van ladingsdragers heeft en dus een lagere geleidbaarheid.
Samenvattend: Zoutwater heeft meer opgeloste ionen, die fungeren als ladingsdragers, wat leidt tot een veel hogere geleidbaarheid in vergelijking met leidingwater.
 Waarom geometrie van H2O is niet lineair, terwijl CO2 lineair is?
Waarom geometrie van H2O is niet lineair, terwijl CO2 lineair is?  Wat is het getal op het periodiek systeem voor HCl?
Wat is het getal op het periodiek systeem voor HCl?  Schrijf het elektronenconfiguratiediagram dat de overdracht van elektronen weergeeft, vindt plaats om samengesteld natriumfluoride te vormen en ionen gevormd ionen op te nemen?
Schrijf het elektronenconfiguratiediagram dat de overdracht van elektronen weergeeft, vindt plaats om samengesteld natriumfluoride te vormen en ionen gevormd ionen op te nemen?  Vervuilers, ziekteverwekkers kunnen samenwerken om ons ziek te maken
Vervuilers, ziekteverwekkers kunnen samenwerken om ons ziek te maken Lachgas Hoe werkt
Lachgas Hoe werkt
 Verder zoeken dan seismologie naar voorlopers van aardbevingen
Verder zoeken dan seismologie naar voorlopers van aardbevingen Groot onderzoek naar de opwarming van de aarde opnieuw in twijfel getrokken, opnieuw verdedigd
Groot onderzoek naar de opwarming van de aarde opnieuw in twijfel getrokken, opnieuw verdedigd NASA volgt zware regenval Beta's in lagere Mississippi-vallei
NASA volgt zware regenval Beta's in lagere Mississippi-vallei Meteorologen verbeteren multivariabele geïntegreerde evaluatiemethode voor klimaatmodel
Meteorologen verbeteren multivariabele geïntegreerde evaluatiemethode voor klimaatmodel Wie bestudeert de omgeving en middelen van aardes?
Wie bestudeert de omgeving en middelen van aardes?
Hoofdlijnen
- Wat leidt de natuurlijke selectie tot de evolutie van?
- Welk organisme wordt gebruikt om gisting te bestuderen?
- Wat is de menselijke functie?
- Zijn geniale en krankzinnigheid op hetzelfde chromosoom?
- Site waar ribosomaal RNA wordt gemaakt?
- Kunnen katten op een plaats delict helpen bij het vinden van belangrijk DNA-bewijs?
- Wat is fenolftaleïne?
- Welk type sporen produceren lycopodium?
- Kunnen we de thylacine weer tot leven wekken? Misschien, maar het zal de mondiale uitstervingscrisis niet helpen
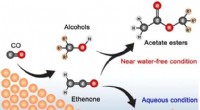
- Duurzame elektrosynthese van esters
- Technieken voor het observeren van beton terwijl het hard wordt, kunnen de ontwikkeling van nieuw cement vergemakkelijken

- Nieuw centrum om olie en gas te vervangen door duurzame chemie

- Ingenieursreactor zet gas direct om in azijnzuur

- Onderzoekers ontwikkelen nieuwe materialen voor energie en detectie

 Welke elementen reageren met zoutzuur?
Welke elementen reageren met zoutzuur?  Welke structuur in levende organismen is gemaakt van fosfolipiden?
Welke structuur in levende organismen is gemaakt van fosfolipiden?  Wat is de gebalanceerde vergelijking voor vaste calcium reageert met waterig salpeterzuur om nitraat en waterstofgas te vormen?
Wat is de gebalanceerde vergelijking voor vaste calcium reageert met waterig salpeterzuur om nitraat en waterstofgas te vormen?  Waarom moet een ruimtevaartuig een ontsnappingssnelheid bereiken om ruimte te kunnen hebben?
Waarom moet een ruimtevaartuig een ontsnappingssnelheid bereiken om ruimte te kunnen hebben?  Een interdecadale afname van dagen met extreme hitte in augustus boven Noordoost-China rond het begin van de jaren negentig
Een interdecadale afname van dagen met extreme hitte in augustus boven Noordoost-China rond het begin van de jaren negentig Een regenboog van kleuren verfijnen op nanoschaal
Een regenboog van kleuren verfijnen op nanoschaal Wie heeft de rotatie en de revolutie ontdekt?
Wie heeft de rotatie en de revolutie ontdekt?  Een nieuwe draai aan de oorsprong van het leven?
Een nieuwe draai aan de oorsprong van het leven?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

