
Wetenschap
Waarom hebben waterstofatomen in water een lichte positieve lading?
Hier is een uitsplitsing:
* zuurstof is meer elektronegatief dan waterstof. Dit betekent dat zuurstof een sterkere trek heeft op gedeelde elektronen in de covalente bindingen die het vormt met waterstof.
* ongelijke delen van elektronen: Als gevolg hiervan brengen de gedeelde elektronen meer tijd dichter bij het zuurstofatoom door, waardoor de zuurstof een enigszins negatieve lading (Δ-) krijgt en de waterstofatomen met een enigszins positieve lading (δ+) achterlaten.
* Polair molecuul: Deze ongelijke ladingsverdeling maakt het watermolecuul polair , wat betekent dat het een positief en negatief einde heeft.
De structuur van het watermolecuul draagt verder bij aan deze polariteit:
* gebogen vorm: De twee waterstofatomen worden gebonden aan het zuurstofatoom onder een hoek van ongeveer 104,5 graden, waardoor het watermolecuul een gebogen of V-vormige geometrie krijgt. Deze vorm versterkt de ongelijke ladingsverdeling en plaatst de positieve ladingen aan de ene kant van het molecuul en de negatieve lading aan de andere kant.
Deze lichte positieve lading op de waterstofatomen in water is belangrijk voor veel biologische processen, waaronder:
* waterstofbinding: De positieve waterstofatomen kunnen waterstofbruggen vormen met andere elektronegatieve atomen, zoals zuurstof of stikstof, in andere moleculen. Deze binding is cruciaal voor het bij elkaar houden van grote biomoleculen zoals eiwitten en DNA.
* Oplosbaarheid: Door de polaire aard van water kan het veel polaire en ionische stoffen oplossen, waardoor het een uitstekend oplosmiddel is voor biologische processen.
Laat het me weten als je nog meer vragen hebt!
Hoofdlijnen
- Kunnen ziektedetecterende honden de dikhoornschapen in South Dakota helpen redden?
- Anatomische structuren: homoloog, analoog & vestigiaal
- Is een kristal abiotisch of biotisch?
- Zouttolerante planten kweken
- Hoe de varkensgriep werkt
- Waar zijn de chromosomen gelegen in een normale cel?
- Onderzoekers laten zien dat cellen communiceren door gebruik te maken van een glasvezelnetwerk
- Op welk proces worden nieuwe cellen gemaakt?
- Wat doet ons gapen?
- Onderzoeksteam ontdekt gebruik van elasticiteit om microplaten op gebogen 2D-vloeistoffen te positioneren
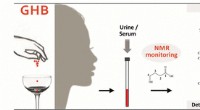
- De detectie van een date rape drug verbeteren
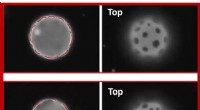
- Nieuwe aanpak creëert een uitzonderlijke katalysator met één atoom voor watersplitsing

- Onderzoek toont aan dat keramiek kan vervormen als metalen als het onder een elektrisch veld wordt gesinterd

- Nieuwe methode kan helpen onaangeboorde aardgasreservoirs te kwantificeren

 Terwijl zonne-energie de krantenkoppen haalt, appartementsbewoners vinden duurzaamheidsopties
Terwijl zonne-energie de krantenkoppen haalt, appartementsbewoners vinden duurzaamheidsopties Filippijnse enquête toont schokkend plastic afval
Filippijnse enquête toont schokkend plastic afval Zorgen voor wereldwijde voedselzekerheid tijdens COVID-19
Zorgen voor wereldwijde voedselzekerheid tijdens COVID-19 Wat is de pH van ammoniumjodide?
Wat is de pH van ammoniumjodide?  Waarom zie je niet elke dag een volle maan?
Waarom zie je niet elke dag een volle maan?  Waarom veroorzaakt ruwe olie problemen aan de korst?
Waarom veroorzaakt ruwe olie problemen aan de korst?  De Saltonzee in Zuid-Californië stinkt nu het hele jaar door en verergert het astma van mensen:de boosdoener? Bacteriën
De Saltonzee in Zuid-Californië stinkt nu het hele jaar door en verergert het astma van mensen:de boosdoener? Bacteriën  Het gedrag van primaten veranderde toen dierentuinen gesloten waren wegens pandemie, suggereert onderzoek
Het gedrag van primaten veranderde toen dierentuinen gesloten waren wegens pandemie, suggereert onderzoek
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


