
Wetenschap
Wat is het proces als een vaste stof in gas verandert?
1. Energieabsorptie:
* Vaste deeltjes hebben een vaste opstelling en worden bij elkaar gehouden door sterke intermoleculaire krachten.
* Wanneer voldoende warmte -energie wordt geabsorbeerd door de vaste stof, krijgen de deeltjes kinetische energie en beginnen ze sneller te trillen.
2. Intermoleculaire krachten overwinnen:
* Naarmate de kinetische energie toeneemt, worden de trillingen zo sterk dat ze de intermoleculaire krachten overwinnen die de deeltjes bij elkaar houden.
* De deeltjes breken los van hun vaste structuur.
3. Overgang naar gas:
* De bevrijde deeltjes bewegen nu willekeurig en onafhankelijk en vullen de beschikbare ruimte.
* Dit is de gasvormige toestand, waar de deeltjes ver uit elkaar liggen en zwakke intermoleculaire krachten hebben.
Voorbeelden van sublimatie:
* droog ijs (vast koolstofdioxide) sublimeren in kooldioxidegas. Dit is een veel voorkomend voorbeeld, omdat droogijs niet in een vloeibare toestand smelt.
* naftaleen (mottballs) verdwijnen in de loop van de tijd. Het vaste naftaleen sublimeert langzaam in de lucht.
* bevroren water (ijs) verandert in waterdamp (gas) in koude, droge klimaten. Dit is hoe vorst verdwijnt op koude oppervlakken.
Factoren die sublimatie beïnvloeden:
* Temperatuur: Hogere temperaturen bieden meer energie voor de deeltjes om intermoleculaire krachten te overwinnen.
* Druk: Lagere druk zorgt ervoor dat de deeltjes gemakkelijker in de gasvormige toestand kunnen ontsnappen.
* substantie: Verschillende stoffen hebben verschillende sterke punten van intermoleculaire krachten, wat hun gemak van sublimatie beïnvloedt.
Laat het me weten als je nog andere vragen hebt!
 Nieuw rapport beveelt wijzigingen aan in de schattingsmethoden voor gewassen en contante huur die door de NASS worden gebruikt
Nieuw rapport beveelt wijzigingen aan in de schattingsmethoden voor gewassen en contante huur die door de NASS worden gebruikt Enorm Antarctisch ijsblok klaar om af te breken
Enorm Antarctisch ijsblok klaar om af te breken Zijn er voordelen tot leven op het land?
Zijn er voordelen tot leven op het land?  Plant een boom:Milans ambitieuze plannen om schoner te worden, groener
Plant een boom:Milans ambitieuze plannen om schoner te worden, groener NASA werpt een infrarood oog op tropische storm Irwin
NASA werpt een infrarood oog op tropische storm Irwin
Hoofdlijnen
- Hoe vaccins werken
- Onderzoek onderzoekt hoe jonge vissen plastic binnenkrijgen
- Wat wordt het voedsel dat wordt gebruikt in aerobe ademhaling?
- Kunnen schimmels plastic vervangen?
- Het type weefsel dat de Bodys-structuren ondersteunt en vasthoudt
- 3 fasen van interfase
- Wat is wetenschap en tecnologie?
- Herstel van iconische inheemse vogel veroorzaakt problemen in stedelijke gebieden
- Wat zijn de verschillen tussen biologisch en fylogenetisch concept van morfologische soorten?
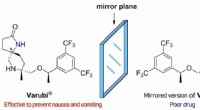
- Nuttige verbindingen synthetiseren zonder ongewenste chirale partners te vormen
- Chemici ontwikkelen veilige alternatieven voor ftalaten die in kunststoffen worden gebruikt

- Eenvoudige methode voorgesteld voor microfabricage op niet-vlakke substraten

- Bacteriële biofilms, beginnen
- Onderzoekers stellen nieuwe technologie voor luchtvaartmaterialen voor om hun eigenschappen aan te passen

 Hoe kun je je 1990 300ZX repareren bij het inschakelen van de lichten aan alleen hi balken werk met geen staart maar stappenrem low gaat uit en dash spedo?
Hoe kun je je 1990 300ZX repareren bij het inschakelen van de lichten aan alleen hi balken werk met geen staart maar stappenrem low gaat uit en dash spedo?  Europa's oudste boom groeit nog steeds
Europa's oudste boom groeit nog steeds  Hoeveel pond is 3,7 gram gelijk?
Hoeveel pond is 3,7 gram gelijk?  Schijnt de zon op Uranus?
Schijnt de zon op Uranus?  Wat is de positie van de aarde in het zonnestelsel?
Wat is de positie van de aarde in het zonnestelsel?  Studies over massale schietpartijen beoordelen trends, effectiviteit meten, en beleid aanbevelen
Studies over massale schietpartijen beoordelen trends, effectiviteit meten, en beleid aanbevelen Wat voor soort reaactie heeft altijd zuurstof als een reactant?
Wat voor soort reaactie heeft altijd zuurstof als een reactant?  Wat zijn voorbeelden van niet-vloeistoffen?
Wat zijn voorbeelden van niet-vloeistoffen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

