
Wetenschap
Waarom worden overgangsmetaal grotendeels gebruikt als katalysator?
1. Variabele oxidatietoestanden:
Overgangsmetalen hebben meerdere oxidatietoestanden, waardoor ze gemakkelijk elektronen kunnen winnen of verliezen. Dit maakt ze goed in het vormen van tijdelijke bindingen met reactanten, waardoor chemische reacties worden vergemakkelijkt.
2. Mogelijkheid om complexen te vormen:
Ze vormen gemakkelijk complexen met liganden, die moleculen of ionen zijn die binden aan het metaalion. Deze complexen kunnen worden aangepast om specifieke katalytische activiteit te bieden, de reactieroute te regelen en de efficiëntie ervan te verbeteren.
3. D-Orbitals:
Overgangsmetalen hebben gedeeltelijk gevulde D-orbitalen, die betrokken zijn bij de binding en de juiste energieniveaus hebben om elektronen te accepteren of te doneren tijdens reacties. Dit zorgt voor gemakkelijkere elektronenoverdracht en vergemakkelijkt de katalyse.
4. Oppervlakte:
Veel overgangsmetalen kunnen bestaan in fijn verdeelde vormen en bieden een groot oppervlak voor interactie met reactanten. Dit verhoogt de reactiesnelheid door meer locaties te bieden voor adsorptie en katalyse.
5. Elektronische structuur:
Hun elektronische structuur stelt hen in staat om gemakkelijk zowel Sigma- als PI -bindingen te vormen, waardoor ze veelzijdigheid krijgen in interactie met verschillende soorten reactanten.
Voorbeelden van overgangsmetaalkatalysatoren:
* nikkel: Gebruikt bij hydrogenatiereacties, zoals de omzetting van alkenen in alkanen.
* ijzer: Werkzaam in het Haber-Bosch-proces voor ammoniaksynthese.
* platina: Vaak gebruikt in katalytische converters om schadelijke emissies van auto's te verminderen.
* palladium: Toegepast in verschillende organische reacties, waaronder cross-koppelingsreacties.
* rhodium: Bekend om zijn rol in hydroformyleringsreacties, waarbij alkenen worden omgezet in aldehyden.
Voordelen van het gebruik van overgangsmetaalkatalysatoren:
* Verhoogde reactiesnelheden: Katalysatoren versnellen de reacties, wat leidt tot snellere en efficiëntere processen.
* Lagere activeringsenergie: Overgangsmetalen verlagen de activeringsenergie die nodig is voor een reactie, waardoor het gemakkelijker is om op te treden.
* selectiviteit: Ze kunnen worden ontworpen om specifieke reacties te bevorderen, wat leidt tot gewenste producten.
* milieuvoordelen: Ze maken het vaak mogelijk dat reacties optreden onder mildere omstandigheden, waardoor het energieverbruik en het afval worden verminderd.
Over het algemeen maken de unieke elektronische en structurele eigenschappen van overgangsmetalen ze zeer effectieve katalysatoren. Hun vermogen om elektronenoverdracht te vergemakkelijken, complexen te vormen en op verschillende manieren te interageren met reactanten stelt hen in staat om een cruciale rol te spelen in diverse chemische processen.
 Kustwateren zijn onverwachte hotspots voor stikstofbinding
Kustwateren zijn onverwachte hotspots voor stikstofbinding Welke discipline is landonderzoek?
Welke discipline is landonderzoek?  Hoe van het land te leven... in een grote Amerikaanse stad
Hoe van het land te leven... in een grote Amerikaanse stad Een terugblik op recordbrekende mei-yu-regenval en overstromingen in 2020 in heel China
Een terugblik op recordbrekende mei-yu-regenval en overstromingen in 2020 in heel China Twee manieren waarop bladeren worden aangepast om de evaperatie van water te verminderen?
Twee manieren waarop bladeren worden aangepast om de evaperatie van water te verminderen?
Hoofdlijnen
- Hoe correleren de verschillende takken van biologie of correleren ze met elkaar?
- Wat is de verschil van een dipliod en hapliod -cel?
- Het oversteken van organismen van de F1 -generatie produceert welke generatie?
- Definieer alstublieft een resistent -kolonie vanuit het oogpunt van microbiologie?
- Wetenschappers leggen uit hoe chromosomen zich reorganiseren na celdeling
- Kymatologie is de studie van wat?
- Welke woorden hebben een wetenschappelijke connotatie?
- Honden zijn overleden na het likken van een gewone chemotherapiecrème, waarschuwt de FDA
- Is het bevruchte ei een eencellulair organisme?
- Onderzoekers ontdekken structuur van anti-verouderingshormoon
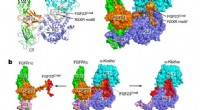
- Nieuwe chemische modificatie van een natuurlijke verbinding voor de behandeling van kanker

- Onderzoekers stellen vast hoe sorptiematerialen koolstof vangen en afgeven

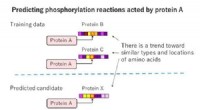
- Fujitsu ontwikkelt technologie om biochemische reacties te voorspellen, opheldering van de mechanismen van genetische aandoeningen
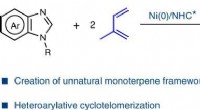
- Wetenschappers realiseren door nikkel gekatalyseerde asymmetrische heteroarylatieve cyclotelomerisatie van isopreen
 Uit welk mineraal bestaan stalactieten en stalagmieten?
Uit welk mineraal bestaan stalactieten en stalagmieten?  Gecertificeerde duurzame palmolievelden vormen al meer dan 30 jaar een gevaar voor leefgebieden van zoogdieren en biodiverse tropische bossen
Gecertificeerde duurzame palmolievelden vormen al meer dan 30 jaar een gevaar voor leefgebieden van zoogdieren en biodiverse tropische bossen Observaties van de jonge ster vertellen ons dat wanneer de zon zonnewind was?
Observaties van de jonge ster vertellen ons dat wanneer de zon zonnewind was?  Hoe goede darmbacteriën het risico op hartaandoeningen helpen verminderen
Hoe goede darmbacteriën het risico op hartaandoeningen helpen verminderen Californisch eiland Catalina krijgt close-up met nieuwe macOS
Californisch eiland Catalina krijgt close-up met nieuwe macOS Isolator-metaalovergang op nanoschaal
Isolator-metaalovergang op nanoschaal Wat is het verschil tussen luchtsnelheid en grondsnelheid?
Wat is het verschil tussen luchtsnelheid en grondsnelheid?  Echt? De meeste Amerikanen hebben geen last van een informatie-overload
Echt? De meeste Amerikanen hebben geen last van een informatie-overload
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

