
Wetenschap
Hoe gedragen de moleculen van een gas zich?
1. Constante willekeurige beweging: Gasmoleculen zijn in constante, willekeurige beweging. Dit betekent dat ze in alle richtingen bewegen en bij verschillende snelheden, botsen met elkaar en de wanden van hun container.
2. Verwaarloosbare intermoleculaire krachten: In tegenstelling tot vloeistoffen en vaste stoffen hebben gasmoleculen zeer zwakke aantrekkelijke krachten ertussen. Dit komt omdat ze ver uit elkaar liggen en snel bewegen, dus hun interacties zijn kort en zwak.
3. Hoge samendrukbaarheid: Gassen zijn zeer samendrukbaar, wat betekent dat hun volume aanzienlijk kan worden verminderd door druk uit te oefenen. Dit komt omdat de moleculen breed op elkaar zijn geplaatst, waardoor veel lege ruimte tussen hen achterblijft.
4. Uitbreiding om hun container te vullen: Gassen zullen uitbreiden om het gehele volume van hun container te vullen. Dit komt omdat de moleculen voldoende energie hebben om hun zwakke intermoleculaire krachten te overwinnen en zich te verspreiden.
5. Diffusie en effusie: Gassen vertonen diffusie, wat betekent dat ze kunnen mengen met andere gassen. Ze ondergaan ook effusie, het proces van een gas dat door een klein gat in een vacuüm ontsnapt. De snelheid van effusie is omgekeerd evenredig met de vierkantswortel van de molaire massa van het gas (de wet van Graham).
6. Lage dichtheid: Gassen hebben een lage dichtheid in vergelijking met vloeistoffen en vaste stoffen omdat hun moleculen worden verspreid, wat leidt tot minder massa per volume -eenheid.
7. Kinetische energie: Gasmoleculen bezitten kinetische energie vanwege hun constante beweging. De gemiddelde kinetische energie van de moleculen is recht evenredig met de absolute temperatuur van het gas.
8. Druk: De druk die door een gas wordt uitgeoefend, is het gevolg van de botsingen van gasmoleculen met de wanden van hun container. De druk neemt toe met toenemende temperatuur en dichtheid.
9. Ideaal gasgedrag: Hoewel echte gassen afwijken van ideaal gedrag, vooral bij hoge drukken en lage temperaturen, biedt de ideale gaswet een goede benadering voor het gedrag van veel gassen onder normale omstandigheden. De ideale gaswet stelt dat PV =NRT, waarbij P druk is, V is volume, N is het aantal mol, r is de ideale gasconstante en T is temperatuur.
Het begrijpen van deze eigenschappen is cruciaal voor het begrijpen van het gedrag van gassen in verschillende toepassingen, waaronder atmosferische wetenschap, chemische reacties en engineering.
 Een nieuwe manier om te zien of die plastic fles of zak gerecycled materiaal bevat
Een nieuwe manier om te zien of die plastic fles of zak gerecycled materiaal bevat Wat zullen de deeltjes doen als metaal door ijs wordt afgekoeld?
Wat zullen de deeltjes doen als metaal door ijs wordt afgekoeld?  Zijn koolstofdioxide en tetrachloride de enige twee niet -polaire moleculen?
Zijn koolstofdioxide en tetrachloride de enige twee niet -polaire moleculen?  Waar begint de nucleolus uiteen te vallen?
Waar begint de nucleolus uiteen te vallen?  Wat is de woordvergelijking voor fenol- en broomwater?
Wat is de woordvergelijking voor fenol- en broomwater?
 Wat is de onderste laag van het regenwoud?
Wat is de onderste laag van het regenwoud?  Klimaat uitgelegd:hoe regelingen voor emissiehandel ons kunnen helpen over te schakelen naar een koolstofvrije toekomst
Klimaat uitgelegd:hoe regelingen voor emissiehandel ons kunnen helpen over te schakelen naar een koolstofvrije toekomst Verspil het kapitaal van de natuur niet:David Attenborough
Verspil het kapitaal van de natuur niet:David Attenborough Verkeer bleek een belangrijke bron van atmosferische nanocluster-aerosolen
Verkeer bleek een belangrijke bron van atmosferische nanocluster-aerosolen Modelvergelijking voegt meer waarde toe bij het simuleren van extreme temperaturen in China
Modelvergelijking voegt meer waarde toe bij het simuleren van extreme temperaturen in China
Hoofdlijnen
- Hoe slimme luiers kunnen helpen bij het ontwikkelen van nieuwe wapens in de strijd tegen bacteriën
- Is uw hond agressief? Een dierenarts legt het woedesyndroom uit
- Verbetering van de hittetolerantie in graszoden in het koele seizoen
- Het is onthuld dat liefdeshormoon hartgenezende eigenschappen heeft
- Wat is de bestelling auditieve botten trillen?
- Bloem of kracht? Actievoerders vrezen dat de lithiummijn zeldzame planten kan doden
- De enige factor die een wetenschapper verandert tijdens een experiment, ook wel onafhankelijke variabele genoemd?
- Wat komt voornamelijk uit de kerncel?
- Wat zijn fenotype en genotype Welke termen die ze beschrijven?
- Hoe een kristallijne spons watermoleculen afstoot

- De rol van vastestofchemie bij de ontwikkeling van metaal-ionbatterijen

- Historische films kunnen dankzij het azijnsyndroom veel sneller vergaan dan we dachten

- Transplantatiebeschadigend virus komt in beeld
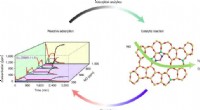
- Ingenieurs lossen mysterie op van de relatie tussen structuur en eigenschappen in katalysatoren voor emissiebeheersing
 Welke handschoenen moeten worden gebruikt voor het omgaan met aceton?
Welke handschoenen moeten worden gebruikt voor het omgaan met aceton?  Hoeveel kiezers wisselen werkelijk van partij bij de Britse verkiezingen? Wat het bewijsmateriaal ons vertelt
Hoeveel kiezers wisselen werkelijk van partij bij de Britse verkiezingen? Wat het bewijsmateriaal ons vertelt  Waar zijn plantes van gemaakt?
Waar zijn plantes van gemaakt?  Experiment met klimaatopwarming vindt onverwachte resultaten
Experiment met klimaatopwarming vindt onverwachte resultaten Wetenschapper aan het werk:ik ben een geoloog die tientallen keren heeft gedoken om onderzeese vulkanen te verkennen
Wetenschapper aan het werk:ik ben een geoloog die tientallen keren heeft gedoken om onderzeese vulkanen te verkennen Sterrenwetten:wat gebeurt er als je een misdaad in de ruimte pleegt?
Sterrenwetten:wat gebeurt er als je een misdaad in de ruimte pleegt? Hoe zuurstof de kern van belangrijke enzymen vernietigt
Hoe zuurstof de kern van belangrijke enzymen vernietigt  Inktvisinkt veelbelovend gevonden voor de behandeling van kanker
Inktvisinkt veelbelovend gevonden voor de behandeling van kanker
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

