
Wetenschap
Vormt deuterium in D2O waterstofbruggen?
Dit is waarom:
* waterstofbinding: Waterstofbinding treedt op wanneer een waterstofatoom wordt gebonden aan een sterk elektronegatief atoom (zoals zuurstof in water). Het waterstofatoom ontwikkelt een gedeeltelijke positieve lading, terwijl de zuurstof een gedeeltelijke negatieve lading ontwikkelt. Dit creëert een sterke elektrostatische aantrekkingskracht tussen de waterstof van het ene molecuul en de zuurstof van een ander molecuul.
* deuterium: Deuterium (D) is een isotoop van waterstof, die één proton en één neutron bevat. Het gedraagt zich chemisch bijna identiek aan waterstof, met slechts enigszins verschillende eigenschappen vanwege de zwaardere massa.
* D2O vs. H2O: Het verschil in massa tussen deuterium en waterstof heeft geen significante invloed op het vermogen om waterstofbruggen te vormen. De elektronegativiteit van zuurstof en de gedeeltelijke ladingen op waterstof en zuurstof blijven vergelijkbaar in D2O.
Daarom kan deuterium in D2O waterstofbruggen vormen met zuurstofatomen in andere D2O -moleculen, net als waterstof in H2O.
De sterkte en dynamiek van waterstofbruggen in D2O zijn echter iets anders dan H2O vanwege de zwaardere massa deuterium. Deze verschillen kunnen leiden tot enkele interessante effecten, zoals een iets hoger kookpunt voor D2O.
 Lavalamptektoniek:hoe gigantische klodders ondergedompeld sediment door de diepe aarde omhoog drijven
Lavalamptektoniek:hoe gigantische klodders ondergedompeld sediment door de diepe aarde omhoog drijven Waar is alles in het universum van gemaakt?
Waar is alles in het universum van gemaakt?  Ontdekkingsreiziger om de stroom van plastic langs 10 rivieren in zeeën te traceren
Ontdekkingsreiziger om de stroom van plastic langs 10 rivieren in zeeën te traceren Waarom wordt intelligent ontwerp niet algemeen geaccepteerd als een wetenschappelijke verklaring voor de oorsprong van het leven op aarde?
Waarom wordt intelligent ontwerp niet algemeen geaccepteerd als een wetenschappelijke verklaring voor de oorsprong van het leven op aarde?  Hoe op de natuur gebaseerde oplossingen effectief overstromingsbeheer kunnen bevorderen
Hoe op de natuur gebaseerde oplossingen effectief overstromingsbeheer kunnen bevorderen
Hoofdlijnen
- Waarom zijn sommige mensen muggenmagneten en anderen niet? Entomoloog wijst op stofwisseling, lichaamsgeur en mindset
- Wat zijn door vesicle gemedieerd transport is een soort van?
- Hoe is de persoon die de fysieke wetenschap bestudeert?
- Soorten organellen
- Welke manier stroomt de genetische informatie?
- 3 weefsels die het vasculaire systeem vormen in een zaadplant?
- Wie draagt het verteerde voedsel door alle delen van het lichaam?
- Zijn de eerste cellen geëvolueerd in sodameren?
- Hoe zouden een organisme en zijn cellen worden geholpen door een warme temperatuur?
- Cellulose:een altijd aanwezig materiaal met opmerkelijke eigenschappen
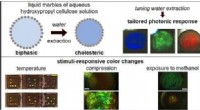
- Wetenschappers laten onderzoekshydrogel meer als biologische weefsels groeien

- Herbruikbare stoffen maskers blijven na een jaar wassen goed, drogen

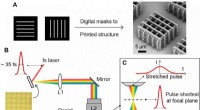
- Nieuwe techniek verhoogt 3D-printsnelheid met 1, 000 tot 10, 000 keer
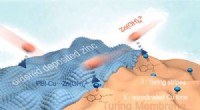
- Turing-membraan om de prestaties van op zink gebaseerde batterijen te verbeteren
 Is Pendulum een voorbeeld van oscillerende beweging?
Is Pendulum een voorbeeld van oscillerende beweging?  Papershow is een draagbaar whiteboard, presentatie en meer
Papershow is een draagbaar whiteboard, presentatie en meer  Stadsplanning voor sub-Sahara Afrikaanse steden heroverwegen
Stadsplanning voor sub-Sahara Afrikaanse steden heroverwegen Wetenschappers passen twistronics toe op de voortplanting van licht en doen een baanbrekende ontdekking
Wetenschappers passen twistronics toe op de voortplanting van licht en doen een baanbrekende ontdekking Hoe elektriciteit werkt
Hoe elektriciteit werkt  Reageert ijzer met salpeterzuur?
Reageert ijzer met salpeterzuur?  Wat zijn de 10 biologische takken van de wetenschap?
Wat zijn de 10 biologische takken van de wetenschap?  Uniek beeld verkregen door wetenschappers met hogesnelheidscamera laat zien hoe bliksemafleiders werken
Uniek beeld verkregen door wetenschappers met hogesnelheidscamera laat zien hoe bliksemafleiders werken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

