
Wetenschap
Hoe definieer je de atoomstaat?
1. Energieniveaus:
* Atomen hebben de energieniveaus gekwantiseerd, wat betekent dat elektronen alleen kunnen bestaan bij discrete energiewaarden. Deze niveaus worden vaak weergegeven door getallen zoals 1, 2, 3, enz., Overeenkomstig de grondtoestand (laagste energie) en geëxciteerde toestanden (hogere energie).
2. Elektronenconfiguratie:
* De atomaire toestand van een atoom wordt bepaald door de verdeling van zijn elektronen tussen deze energieniveaus. Een waterstofatoom in zijn grondtoestand heeft bijvoorbeeld zijn enkele elektron in het laagste energieniveau (n =1), terwijl het in een opgewonden toestand zijn elektron op een hoger niveau kan hebben (n =2, 3, enz.).
3. Waarschijnlijkheden:
* Kwantummechanica dicteert dat we de exacte locatie van een elektron op een bepaald moment niet kunnen kennen. In plaats daarvan gebruiken we golffuncties om de kans te beschrijven om een elektron in een bepaald gebiedsgebied te vinden. De atomaire toestand neemt deze kansen op voor elk elektron in het atoom.
4. Notatie:
* Atomische toestanden worden vaak weergegeven met behulp van spectroscopische notatie, waaronder het belangrijkste kwantumnummer (N), het Angular Momentum Quantum -nummer (L) en het spin -kwantumnummer (en) voor elk elektron. De grondtoestand van waterstof wordt bijvoorbeeld weergegeven als 1S1, wat aangeeft dat het enkele elektron zich in de n =1, l =0 en s =1/2 staat.
5. Overgangen:
* Atomen kunnen overgaan tussen verschillende atoomstaten door fotonen van licht te absorberen of uit te stoten. Deze overgangen volgen specifieke selectieregels die bepalen welke veranderingen op energieniveau zijn toegestaan.
Sleutelpunten:
* Atomische toestanden worden gekwantiseerd, wat betekent dat alleen specifieke toestanden mogelijk zijn.
* De atomaire toestand bepaalt de energie, chemische eigenschappen en interacties van het atoom met licht.
* Inzicht in atomaire toestanden is cruciaal op velden zoals spectroscopie, lasertechnologie en kwantumchemie.
In eenvoudiger termen is een atomaire toestand als een momentopname van de interne energieconfiguratie en elektronenverdeling van een atoom. Het is een manier om het energieniveau van het atoom, de elektronenconfiguratie en de kans te beschrijven om zijn elektronen op verschillende locaties te vinden.
 Hoe varieert de afstands- en dichtheidsafhankelijkheid in de levensfasen van planten?
Hoe varieert de afstands- en dichtheidsafhankelijkheid in de levensfasen van planten?  Vermoeide inwoners van Louisiana beoordelen de schade van de laatste orkaan
Vermoeide inwoners van Louisiana beoordelen de schade van de laatste orkaan Wat is het hoofdbestanddeel van de atmosfeer?
Wat is het hoofdbestanddeel van de atmosfeer?  Fossielen die het meest bruikbaar zijn voor correlatie
Fossielen die het meest bruikbaar zijn voor correlatie Wat wordt bedoeld met zonen van de bodem in context voor human resources?
Wat wordt bedoeld met zonen van de bodem in context voor human resources?
Hoofdlijnen
- Wetenschappers ontdekken de mysteries van hoe virussen evolueren
- Het wordt het interne proces genoemd dat voedsel absorbeerbaar maakt?
- Gistonderzoek biedt een mogelijk antwoord op de vraag waarom sommige soorten generalisten zijn en andere specialisten
- Welk type molecuul is het cytoskelet gemeenschappelijk voor alle drie de delen?
- Hoe houdt de huid ziekteverwekkers buiten?
- Factoren die het succes van translocaties van grizzlyberen beïnvloeden
- Nieuwe kaarten laten zien dat de krimpende wildernis op eigen risico wordt genegeerd
- NASA helpt tijgers, jaguars en olifanten te beschermen – zo doe je dat
- Wat is basispaaraffiniteit?
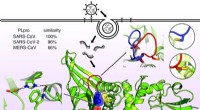
- Informatie over de moleculaire vorm van virussen die COVID-19 veroorzaken, SARS, en MERS onthult structurele overeenkomsten
- Een olie-etende bacterie die vervuiling en morsen kan opruimen

- Onderzoekers rapporteren nieuwe klasse polyethyleenkatalysator

- Nieuwe optische waterstofsensoren elimineren het risico op vonken

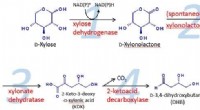
- Metabolic engineering methode slaagt erin om 1, 2, 4-butaantriol duurzaam uit biomassa
 Wetenschappers onthullen structurele geheimen van baleinwalvissen
Wetenschappers onthullen structurele geheimen van baleinwalvissen Waarom zou Biurets -oplossing geel worden?
Waarom zou Biurets -oplossing geel worden?  Waarom sommige nestvogels van Darwin een gele snavel hebben
Waarom sommige nestvogels van Darwin een gele snavel hebben  In vergelijking met de ster is het geëvolueerd uit een witte dwerg?
In vergelijking met de ster is het geëvolueerd uit een witte dwerg?  Top merken gebotteld water verontreinigd met plastic deeltjes:rapport
Top merken gebotteld water verontreinigd met plastic deeltjes:rapport Wat gebeurt er met de aantrekkingskrachten tussen deeltjes als de temperatuur verandert, en waarom?
Wat gebeurt er met de aantrekkingskrachten tussen deeltjes als de temperatuur verandert, en waarom?  31.2 M Squared is gelijk aan hoeveel ft?
31.2 M Squared is gelijk aan hoeveel ft?  Ion biljart cue nieuwe materiaal synthese methode
Ion biljart cue nieuwe materiaal synthese methode
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

