
Wetenschap
Welke groep op het periodiek systeem heeft de meeste stabiele hoeveelheid valentie -elektronen?
Dit is waarom:
* valentie -elektronen: Dit zijn de elektronen in de buitenste schaal van een atoom, die betrokken zijn bij chemische binding.
* stabiliteit: Atomen zijn het meest stabiel wanneer hun buitenste schaal is gevuld met het maximale aantal elektronen dat het kan bevatten.
* Nobele gassen: Nobele gassen hebben een volledige buitenste schaal, wat betekent dat ze een compleet octet (8 valentie -elektronen) hebben, behalve voor helium, dat een compleet duet heeft (2 valentie -elektronen). Dit maakt ze zeer onreactief en stabiel.
Voorbeelden:
* Helium (HE) - 2 valentie -elektronen
* Neon (NE) - 8 valentie -elektronen
* Argon (AR) - 8 valentie -elektronen
* Krypton (KR) - 8 valentie -elektronen
Laat het me weten als je andere groepen en hun stabiliteit wilt verkennen!
 Hoe beïnvloedt het klimaat levens?
Hoe beïnvloedt het klimaat levens?  We hebben geen idee hoeveel microplastic er in de bodem van Australië zit (maar het kan veel zijn)
We hebben geen idee hoeveel microplastic er in de bodem van Australië zit (maar het kan veel zijn) Onderzoekers vinden bewijs van verkeersvervuiling in afgelegen Himalaya
Onderzoekers vinden bewijs van verkeersvervuiling in afgelegen Himalaya Een nieuwe soort zwarte keverlarven die plastic afbreken
Een nieuwe soort zwarte keverlarven die plastic afbreken Wat zijn relatief kleine rotsachtige objecten die rond de zon draaien?
Wat zijn relatief kleine rotsachtige objecten die rond de zon draaien?
Hoofdlijnen
- Chromosoom is kern als DNA tot?
- Het geroezemoes over eetbare insecten:kunnen ze rundvlees vervangen?
- Heeft de pH van water invloed op groeireparaten?
- Vlezige structuur rondom het zaad in een angiosperm?
- Wat is er zo speciaal aan een gespecialiseerde sonde?
- Voerrelaties in ecosystemen worden het best vertegenwoordigd door wat?
- Albuminen zijn de plasma-eiwitten die verantwoordelijk zijn voor?
- Is de kiemtheorie en cel hetzelfde?
- Welke ziekten zijn het gevolg van een abnormale celfunctie?
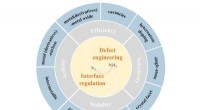
- Defect- en interface-engineering voor e-NRR onder omgevingsomstandigheden
- Methanolsynthese:inzicht in de structuur van een raadselachtige katalysator

- Een katalytisch ondersteunend materiaal speelt een hoofdrol

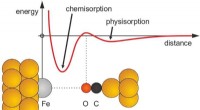
- Aanvankelijke afstoting bij chemische binding sluit latere aantrekking niet uit
- Een nieuwe methode voor de productie van geprotoneerde waterstof

 Boeren zullen profiteren van een nieuwe methode voor het monitoren van weidevoedingsstoffen
Boeren zullen profiteren van een nieuwe methode voor het monitoren van weidevoedingsstoffen Een verhoogde focus op voedselzekerheid en duurzaamheid
Een verhoogde focus op voedselzekerheid en duurzaamheid Wat beschrijft het beste de korst in de wetenschap?
Wat beschrijft het beste de korst in de wetenschap?  Welke chemische elementen zijn te vinden in augurken?
Welke chemische elementen zijn te vinden in augurken?  Wat hondeneigenaren moeten weten over leptospirose
Wat hondeneigenaren moeten weten over leptospirose  Voorganger van de Melkwegbalk?
Voorganger van de Melkwegbalk?  De zon bereikt het hoogtepunt van haar activiteit. Hier ziet u hoe dit meer aurorae en zonnestormen kan veroorzaken
De zon bereikt het hoogtepunt van haar activiteit. Hier ziet u hoe dit meer aurorae en zonnestormen kan veroorzaken  Welke uitvinding helpt ons cel te zien?
Welke uitvinding helpt ons cel te zien?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

