
Wetenschap
Wat voor soort binding is de resultaatoverdracht een elektron?
Dit is waarom:
* elektronenoverdracht: In een ionische binding verliest één atoom (meestal een metaal) een elektron en wordt een positief geladen ion (kation). Het andere atoom (meestal een niet -metaal) wint dat elektron en wordt een negatief geladen ion (anion).
* Elektrostatische aantrekkingskracht: De tegenovergestelde ladingen van het kation en anion trekken elkaar sterk aan, waardoor een sterke elektrostatische kracht ontstaat die de ionen bij elkaar houdt in een kristalroosterstructuur.
Voorbeeld: In tafelzout (NaCl) verliest natrium (NA) een elektron om een natriumion (Na+) te worden, terwijl chloor (CL) dat elektron laat een chloride-ion worden (Cl-). De elektrostatische aantrekkingskracht tussen deze tegengesteld geladen ionen creëert de ionische binding die natriumchloride vormt.
 Bijdrage van Johann DoBereiner voor de periodieke tabel?
Bijdrage van Johann DoBereiner voor de periodieke tabel?  Wat gebeurt er als broomthymolblauw wordt blootgesteld aan CO2?
Wat gebeurt er als broomthymolblauw wordt blootgesteld aan CO2?  Stabiliserend molecuul kan de weg vrijmaken voor lithium-luchtbrandstofcel
Stabiliserend molecuul kan de weg vrijmaken voor lithium-luchtbrandstofcel Welke stof is geen element water zuurstof koolstof chloor waterstof?
Welke stof is geen element water zuurstof koolstof chloor waterstof?  Welke base wordt gevormd als natriumoxide met water reageert?
Welke base wordt gevormd als natriumoxide met water reageert?
 Hoeveel fluor is te veel fluor?
Hoeveel fluor is te veel fluor? Verwoesting terwijl orkaan Irma het Caribisch gebied teistert
Verwoesting terwijl orkaan Irma het Caribisch gebied teistert Hoe verandert de natuur als Persephone beweegt tussen de aarde en de onderwereld?
Hoe verandert de natuur als Persephone beweegt tussen de aarde en de onderwereld?  Verbruikt metaal langzaam wanneer de rijkdom van een land groeit? Misschien niet, studie toont
Verbruikt metaal langzaam wanneer de rijkdom van een land groeit? Misschien niet, studie toont Nieuw inzicht van koraal uit het Great Barrier Reef biedt correctiefactor voor klimaatrecords
Nieuw inzicht van koraal uit het Great Barrier Reef biedt correctiefactor voor klimaatrecords
Hoofdlijnen
- Welke cel bevat chloroplasten die chlorofyl heeft?
- Nieuw onderzoek onthult hoe vleermuishersenen zijn georganiseerd voor echolocatie en vlucht
- Wat beschrijft het beste hoe chromosomen tijdens mitose naar de polen van de spil bewegen?
- Wat is het Human Epigenome Project?
- Evolutie hoe werkt
- Het leven is niet 2D, dus waarom zouden onze encyclopedieën dat wel moeten zijn?
- Wat is de rol van mRNA bij de eiwitsynthese?
- Hoe verschilt de wetenschappelijke methode van religie?
- Waarom worden mitrochondria de krachtpatoren van cellen genoemd?
- Slimme spons kan olielekkages opruimen

- Isolerende stenen met microscopisch kleine belletjes

- Actie van geneesmiddelverbindingen in weefsel onthuld door nieuwe techniek
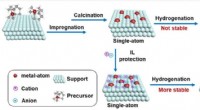
- Wetenschappers ontwikkelen strategie om afzonderlijke atomen te stabiliseren met ionische vloeistof als elektronische stabilisator
- Surrey bouwt AI om chemische verbindingen tegen veroudering te vinden

 Blanke hypotheekagenten kunnen minderheidsleners hogere hypotheekkosten in rekening brengen
Blanke hypotheekagenten kunnen minderheidsleners hogere hypotheekkosten in rekening brengen Bezos-zaak onthult kwetsbaarheid miljardairs voor hackers
Bezos-zaak onthult kwetsbaarheid miljardairs voor hackers Hoe vernietig je een magneet met verwarming of bevriezende methood?
Hoe vernietig je een magneet met verwarming of bevriezende methood?  Wordt magma gevonden in de bovenste mantel?
Wordt magma gevonden in de bovenste mantel?  Hoe maak je je eigen wetenschap Lab
Hoe maak je je eigen wetenschap Lab Wat is de overste conclusie van binnenvlaktes?
Wat is de overste conclusie van binnenvlaktes?  Hoe gebruik je elke dag wetenschap en technologie?
Hoe gebruik je elke dag wetenschap en technologie?  Hoe het coronavirus de terroristische dreigingen in de ontwikkelingslanden vergroot
Hoe het coronavirus de terroristische dreigingen in de ontwikkelingslanden vergroot
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

