
Wetenschap
Als de massa water 4,5 keer groter is dan helium, hoe verhoudt een molecuul zich met atoom?
* massa -vergelijking: De verklaring "De massa water is 4,5 keer groter dan helium" vertelt ons over de relatieve massa's van gehele stoffen (water versus helium), geen individuele moleculen of atomen.
* moleculen versus atomen:
* atoom: De kleinste eenheid van een element dat de chemische eigenschappen van dat element behoudt. Voorbeelden:helium (HE), zuurstof (O), waterstof (H).
* molecuul: Twee of meer atomen bij elkaar gehouden door chemische bindingen. Voorbeelden:water (h₂o), zuurstofgas (o₂).
Hier is hoe de vergelijking werkt:
1. helium (HE): Helium is een element en de atomen zijn enkele, onafhankelijke entiteiten.
2. Water (H₂o): Water is een molecuul bestaande uit twee waterstofatomen en één zuurstofatoom dat aan elkaar is gebonden.
Het belangrijkste punt: De massa van een watermolecuul is groter dan de massa van een heliumatoom omdat:
* Een watermolecuul bevat drie atomen (2 waterstof + 1 zuurstof).
* Zuurstofatomen zijn aanzienlijk zwaarder dan heliumatomen.
Samenvattend:
De verklaring over de massa water die groter is dan helium vertelt ons over de totale massa van de stoffen. De vergelijking van een watermolecuul met een heliumatoom gaat echter over het aantal en soorten atomen binnen elk. Een watermolecuul is zwaarder dan een heliumatoom omdat het meer atomen bevat, waaronder een zwaarder zuurstofatoom.
 Welk systeem neemt zuurstof in en laat koolstofdioxide los?
Welk systeem neemt zuurstof in en laat koolstofdioxide los?  Bio-geïnspireerde moleculaire kleurstoffen voor biomedische fluorescerende beeldvorming
Bio-geïnspireerde moleculaire kleurstoffen voor biomedische fluorescerende beeldvorming Waarom is het smeltpunt van zuiver water 44 graden Celsius?
Waarom is het smeltpunt van zuiver water 44 graden Celsius?  Kooldioxide omzetten in methaan met behulp van ijzer en zonlicht
Kooldioxide omzetten in methaan met behulp van ijzer en zonlicht Wat is het belangrijkste onderdeel van aardgas?
Wat is het belangrijkste onderdeel van aardgas?
 Warmere winters bedreigen Britse zwarte bessenteelt
Warmere winters bedreigen Britse zwarte bessenteelt Waarom tegenslagen in de kindertijd van invloed zijn op de manier waarop iemands gedrag wordt beoordeeld
Waarom tegenslagen in de kindertijd van invloed zijn op de manier waarop iemands gedrag wordt beoordeeld  Trans-Pacific reis van atmosferische deeltjes
Trans-Pacific reis van atmosferische deeltjes Wereldwijde de-oxygenatie van de oceaan gekwantificeerd
Wereldwijde de-oxygenatie van de oceaan gekwantificeerd De begraven wetlands van de wereld terugbrengen uit de dood
De begraven wetlands van de wereld terugbrengen uit de dood
Hoofdlijnen
- Wordt de rivierkreeft als een gewervelde of niet -dier beschouwd?
- Waarom cellen de doorgang van ziekten toestaan
- Wat is biokinese?
- Wat maakte de ontwikkeling van de celtheorie mogelijk?
- Waarom classificeren bioloog?
- Wat als je vriendin blauwe ogen heeft, haar genen bevatten één allel voor en bruin dat recessief is, hoe weet je dat?
- Wat voor soort eigenschap is een aanpassing?
- Wat is een fossiel?
- Welke biotische factoren hebben Red Wolf?
- Team ontdekt door licht aangedreven katalysator vormt olefinen voor medicijn, agrochemische productie

- Samenwerking vormt de strategie voor het vasthouden van extracellulaire blaasjes
- Waarom zijn bepaalde zware metalen oké om te eten? (video)

- De kans op succes in de synthetische chemie vergroten
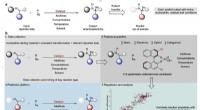
- De opwarming van de aarde aanpakken met nieuwe nanodeeltjes en zonneschijn

 Nylons Eigenschappen & Gebruik
Nylons Eigenschappen & Gebruik  Niets om over te niezen:experimenteel model toont aan dat stuifmeel het weer kan veranderen
Niets om over te niezen:experimenteel model toont aan dat stuifmeel het weer kan veranderen  Hoe 's werelds oudst bekende meteorietinslagstructuur de chemie van de aardkorst veranderde
Hoe 's werelds oudst bekende meteorietinslagstructuur de chemie van de aardkorst veranderde  Een beproefde methode voor het stabiliseren van inspanningen om fusie-energie naar de aarde te brengen
Een beproefde methode voor het stabiliseren van inspanningen om fusie-energie naar de aarde te brengen Nieuw onderzoek onderzoekt hoe duiven gezamenlijke navigatiebeslissingen nemen wanneer ze samen reizen
Nieuw onderzoek onderzoekt hoe duiven gezamenlijke navigatiebeslissingen nemen wanneer ze samen reizen  Hoe maak je een elektroscoop voor een wetenschapsproject
Hoe maak je een elektroscoop voor een wetenschapsproject  Wat is de algemene toestand van sfeer van dag tot belachelijk?
Wat is de algemene toestand van sfeer van dag tot belachelijk?  Hoe ver is Charlotte NC van de evenaar?
Hoe ver is Charlotte NC van de evenaar?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

