
Wetenschap
Wat is de halve reactie van Ba ZnSo4-Baso4 Zn?
1. Identificeer de oxidatie en reductie:
* oxidatie: Zink (Zn) verliest elektronen en de oxidatietoestand neemt toe van 0 tot +2.
* reductie: Barium (BA) krijgt elektronen en zijn oxidatietoestand neemt af van +2 naar 0.
2. Schrijf de halfreacties:
* Oxidatie Halfreactie:
Zn (s) → Zn²⁺ (aq) + 2e⁻
* Reductie halfreactie:
Ba²⁺ (aq) + 2e⁻ → ba (s)
Verklaring:
* Zn (s) → Zn²⁺ (aq) + 2e⁻: Zink verliest in zijn vaste toestand (Zn (S)) twee elektronen om een zinkion (Zn²⁺) in oplossing te worden.
* ba²⁺ (aq) + 2e⁻ → ba (s): Bariumion in oplossing (ba²⁺) krijgt twee elektronen om massief bariummetaal te worden (BA (s)).
Belangrijke opmerking: Het sulfaation (SO₄²⁻) is een toeschouwer -ion in deze reactie. Het neemt niet deel aan de elektronenoverdracht en is niet opgenomen in de halfreacties.
 Wat is het oxidatienummer van HNO2?
Wat is het oxidatienummer van HNO2?  Ontdekking versterkt de theorie dat het leven op aarde is ontstaan uit een RNA-DNA-mix
Ontdekking versterkt de theorie dat het leven op aarde is ontstaan uit een RNA-DNA-mix Mobiel apparaat kan het gemakkelijker maken om schadelijke algenbloei te voorspellen en te beheersen
Mobiel apparaat kan het gemakkelijker maken om schadelijke algenbloei te voorspellen en te beheersen Wetenschappers ontdekken groenere manier om plastic te maken
Wetenschappers ontdekken groenere manier om plastic te maken Hoeveel atomen van hydrogenen zijn er in 3 mol CH4?
Hoeveel atomen van hydrogenen zijn er in 3 mol CH4?
 Klimaatverandering en ontbossing duwen tropische soorten samen richting uitsterven
Klimaatverandering en ontbossing duwen tropische soorten samen richting uitsterven Jaarlijks wordt er op 400.000 Afrikaanse schubdieren gejaagd voor hun vlees – waarom het tijd is om actie te ondernemen
Jaarlijks wordt er op 400.000 Afrikaanse schubdieren gejaagd voor hun vlees – waarom het tijd is om actie te ondernemen  Onderzoek naar hoe ver pollen in de atmosfeer reizen, onthult nieuwe inzichten in oorzaken van stedelijke hooikoorts
Onderzoek naar hoe ver pollen in de atmosfeer reizen, onthult nieuwe inzichten in oorzaken van stedelijke hooikoorts Zijn sprinkhanen schadelijk of nuttig?
Zijn sprinkhanen schadelijk of nuttig?  Verbetering van voorspellingen van hittegolven op zee met geavanceerde assimilatie van oceaangegevens
Verbetering van voorspellingen van hittegolven op zee met geavanceerde assimilatie van oceaangegevens
Hoofdlijnen
- Hoe afval, wildgroei en een opwarmende wereld de muggenseizoenen in Michigan beïnvloeden
- Studie wakkert de discussie aan over waarom vrouwtjesvogels extra partners zoeken
- Wat beschrijft fenotypes het beste?
- Wat zijn niet -voorbeelden van de celcyclus?
- Hoeveel (DNA-)schade kan een kankercel verdragen?
- Wat zijn twee cellen planten en er geen dierencellen?
- Wat is het celproces na meiose of mitose in welke cellen cytoplasma zich verdeelt en scheidt in nieuwe cellen?
- Waar bevinden zich de mitochondriën in de dierlijke cel?
- Interacties tussen microbioomsoorten onthullen hoe bacteriën samenwerken om de dood te bedriegen
- Wetenschappers ontwikkelen body-on-a-chip-systeem om het testen van nieuwe medicijnen te versnellen
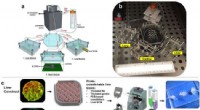
- Het pad van een metallodrug in een borstkankercel onthullen

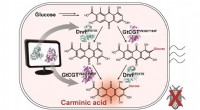
- Microbiële productie van een natuurlijke rode kleurstof karmijnzuur
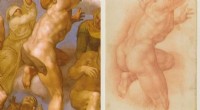
- Nieuwe hydrogel ontwikkeld om tape van eeuwenoude tekening te verwijderen
- De zwavelshuttle stoppen voor betere batterijen

 Nieuwe methode onderzoekt de gas-vloeistof-interface in nieuw detail
Nieuwe methode onderzoekt de gas-vloeistof-interface in nieuw detail Nieuw onderzoek toont aan dat zelfs autoritaire regimes moeite hebben om wetten aan te nemen
Nieuw onderzoek toont aan dat zelfs autoritaire regimes moeite hebben om wetten aan te nemen George Davis Snel
George Davis Snel  Bemanning ruimtestation moet Sojoez verhuizen, maak plaats voor nieuwe bemanningsleden
Bemanning ruimtestation moet Sojoez verhuizen, maak plaats voor nieuwe bemanningsleden Wat zijn alkaanvloeistoffen die continue ketens vormen?
Wat zijn alkaanvloeistoffen die continue ketens vormen?  [APRIL FOOLS DAY!] Onderzoekers creëren Rubiks Cube op moleculaire schaal
[APRIL FOOLS DAY!] Onderzoekers creëren Rubiks Cube op moleculaire schaal Een studie van de grootste maan van Saturnus kan inzichten bieden voor de aarde
Een studie van de grootste maan van Saturnus kan inzichten bieden voor de aarde Wat zijn enkele niet-voorbeelden van chemische energie?
Wat zijn enkele niet-voorbeelden van chemische energie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

