
Wetenschap
Wat is de relatie tussen concentratie van ionen en pH -schaal?
* pH -schaal: De pH -schaal meet de zuurgraad of alkaliteit van een oplossing. Het varieert van 0 tot 14, met:
* 0-6: Zuur
* 7: Neutraal (puur water)
* 8-14: Alkaline (Basic)
* waterstofionen (H+): De zuurgraad is direct gerelateerd aan de concentratie van waterstofionen in een oplossing.
* Hoe meer h+ ionen aanwezig zijn, hoe zure de oplossing.
* Hoe minder H+ ionen aanwezig zijn, hoe meer alkalische (basis) de oplossing.
* De relatie: De pH -schaal is een logaritmische schaal, wat betekent dat elke gehele getalverandering in pH een tienvoudige verandering vertegenwoordigt in de concentratie van waterstofionen:
* Een oplossing met een pH van 4 heeft tien keer meer H+ -ionen dan een oplossing met een pH van 5.
* Een oplossing met een pH van 3 heeft honderd keer meer H+ -ionen dan een oplossing met een pH van 5.
Samenvattend:
* Hoge H+ concentratie =lage pH (zuur)
* lage H+ concentratie =hoge pH (alkalisch)
Voorbeeld:
* Een oplossing met een pH van 3 heeft een waterstofionconcentratie van 10^-3 mol per liter (m).
* Een oplossing met een pH van 10 heeft een waterstofionconcentratie van 10^-10 M.
Belangrijke opmerking: De relatie tussen pH en H+ concentratie is omgekeerd. Naarmate de pH toeneemt, neemt de H+ -concentratie af en vice versa.
 Hoe werkt de hechting op moleculen?
Hoe werkt de hechting op moleculen?  Wat betekent het als een vloeistof in vaste wijze verandert?
Wat betekent het als een vloeistof in vaste wijze verandert?  Onderzoekers ontwikkelen ultrasnelle polymeermodulatoren die tegen de hitte kunnen
Onderzoekers ontwikkelen ultrasnelle polymeermodulatoren die tegen de hitte kunnen Zal naftaleen exploderen als het wordt gemengd met aceton?
Zal naftaleen exploderen als het wordt gemengd met aceton?  Spoor, doelwit, trigger:wetenschappers onderzoeken gecontroleerde CO-afgifte
Spoor, doelwit, trigger:wetenschappers onderzoeken gecontroleerde CO-afgifte
 Hoe hervormen ontleders het landschap?
Hoe hervormen ontleders het landschap?  Wat is de top 3 van natuurlijke hulpbronnen in de VS?
Wat is de top 3 van natuurlijke hulpbronnen in de VS?  Landbouw in Europa neemt af naarmate Aziatische productie groeit:VN, OESO
Landbouw in Europa neemt af naarmate Aziatische productie groeit:VN, OESO De biologische pomp van de oceanen vangt meer koolstof op dan verwacht
De biologische pomp van de oceanen vangt meer koolstof op dan verwacht Veel verontreinigende stoffen in het Noordpoolgebied nemen af na verwijdering en regulering van de markt
Veel verontreinigende stoffen in het Noordpoolgebied nemen af na verwijdering en regulering van de markt
Hoofdlijnen
- Hoe dieren stemmen om groepsbeslissingen te nemen
- Hier ziet u hoe wetenschappers de genetische evolutie van COVID-19 volgen
- Bloem of kracht? Actievoerders vrezen dat de lithiummijn zeldzame planten kan doden
- Hoe wordt de cel in de neus genoemd?
- Koraal selecteert partnerschappen met algen om omgevingsstress te verminderen
- Wat maken wetenschappers om hen te helpen een hypothese of gegevens te verzamelen Durinf -experiment?
- Hoe maken planten zuurstof? Vraag het aan cyanobacteriën
- Is er maar één wetenschappelijke methode.
- Onderzoekers ontdekken hoe weefsels en organen tijdens de embryogenese worden vormgegeven
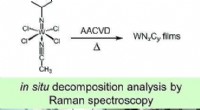
- Gesimuleerde chemische dampafzetting van een wolfraamcarbonitride-precursor
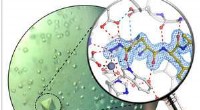
- Inzicht in de structurele en chemische heterogeniteiten van oppervlaktesoorten bij de enkelvoudige bindingslimiet

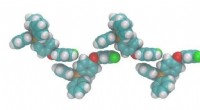
- Dankzij subtiele ioninteracties op moleculair niveau kunnen wetenschappers het smeltpunt van ionische verbindingen afstemmen
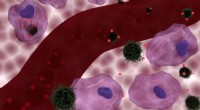
- Warmtebehandeling kan chemotherapie effectiever maken
- Een chemisch maatpak voor alzheimermedicijnen
 Wat is de volledige definitie van plantkunde?
Wat is de volledige definitie van plantkunde?  Verbonden champagne die een kurk in valse bubbels zet
Verbonden champagne die een kurk in valse bubbels zet Welke menselijke activiteiten leiden tot verlies van habitats?
Welke menselijke activiteiten leiden tot verlies van habitats?  Een implanteerbaar apparaat dat energie produceert met behulp van ultrageluid
Een implanteerbaar apparaat dat energie produceert met behulp van ultrageluid 'Magma PI' onthult aanwijzingen over hoe de korst werd gevormd
'Magma PI' onthult aanwijzingen over hoe de korst werd gevormd  Wetenschappers ontwikkelen NIF-optiek van de volgende generatie om energie te verhogen en schade te beperken
Wetenschappers ontwikkelen NIF-optiek van de volgende generatie om energie te verhogen en schade te beperken Wat is grasbankieren?
Wat is grasbankieren?  Tropische storm Humberto richt zich op door orkaan getroffen Bahama's
Tropische storm Humberto richt zich op door orkaan getroffen Bahama's
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

