
Wetenschap
Welke reactie zorgt ervoor dat waterige oplossingen van alkali -metaalcarbonaten basic zijn?
Hier is hoe het werkt:
1. Oplossing: Wanneer een alkalimetaalcarbonaat (zoals natriumcarbonaat, Na₂co₃) in water wordt opgelost, dissocieert het in zijn ionen:
`` `
Na₂co₃ (s) → 2na⁺ (aq) + co₃²⁻ (aq)
`` `
2. Hydrolyse: Het carbonaation (co₃²⁻) reageert met watermoleculen in een omkeerbare reactie:
`` `
Co₃²⁻ (aq) + h₂o (l) ⇌ hco₃⁻ (aq) + oh⁻ (aq)
`` `
3. evenwicht: Deze reactie bereikt evenwicht, maar het bevordert de vorming van bicarbonaationen (HCO₃⁻) en hydroxide -ionen (OH⁻). De hydroxide -ionen (OH⁻) maken de oplossing basic.
In wezen fungeert het carbonaation als een basis door een proton (H⁺) uit water te accepteren, hydroxide -ionen te genereren en de oplossing alkalisch te maken.
Hoofdlijnen
- Water beweegt in floemcellen door osmose en creëert een verhoogde druk die het Sug -water in de rest van de plant duwt. Dit is beschrijving van het verplaatsen van materialen via P?
- Wat betekent communiceren in de wetenschap?
- Verbazingwekkende diversiteit aan soorten gerapporteerd over Solent oesterrestauratieproject
- Wat zijn enkele voorbeelden van organismen die planten planten?
- Waarom kunnen bacteriën menselijke eiwitten produceren?
- Welke stoffen helpen de lichaamsfuncties te reguleren?
- Hoe evolutie werkt
- Muggen dragen bij warm weer vaker het denguevirus over
- Wat zijn voorbeelden van beroepen in de levenswetenschap?
- Vloeibare metalen de geheime ingrediënten om het milieu schoon te maken

- Nieuw katalysatormateriaal produceert overvloedige goedkope waterstof

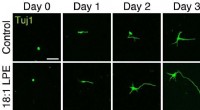
- Oleoyl-LPE oefent neurietstimulatie en neuroprotectie uit
- Moleculaire inzichten in spinnenzijde

- Materiaalinformatica onthult nieuwe klasse van superharde legeringen

 Hoe veranderen bergen in kleine rotsen grond en zand?
Hoe veranderen bergen in kleine rotsen grond en zand?  Wat voor soort binding zou hetzelfde metaal maken?
Wat voor soort binding zou hetzelfde metaal maken?  Digitaal eigendom ontcijferen:waarom uw e-boek misschien niet als 'het uwe' voelt
Digitaal eigendom ontcijferen:waarom uw e-boek misschien niet als 'het uwe' voelt  Waarom vooroordelen over handicaps een bijzonder hardnekkig probleem zijn
Waarom vooroordelen over handicaps een bijzonder hardnekkig probleem zijn Wat is het kookpunt van koolstofatomen?
Wat is het kookpunt van koolstofatomen?  Hoeveel mol zit er in 4,00 g NH3?
Hoeveel mol zit er in 4,00 g NH3?  Licht uit exotische deeltjestoestanden
Licht uit exotische deeltjestoestanden Organismen op het eerste trofische niveau worden genoemd?
Organismen op het eerste trofische niveau worden genoemd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


