
Wetenschap
Waarom worden alkali -metalen bewaard in kerosine?
* zeer reactief: Alkali -metalen hebben een enkel valentie -elektron, waardoor ze extreem reactief zijn. Ze verliezen dit elektron gemakkelijk om positieve ionen te vormen, daarom willen ze zo graag reageren met andere elementen.
* reactie met lucht: Bij blootstelling aan lucht reageren alkali -metalen snel met zuurstof om oxiden te vormen. Deze reactie is exotherme en kan zelfs het metaal ontsteken, waardoor een brand wordt veroorzaakt.
* reactie met water: De reactie van alkali -metalen met water is nog gewelddadiger. Ze reageren krachtig om waterstofgas en een metaalhydroxide te produceren. Deze reactie geeft een significante hoeveelheid warmte vrij, waardoor de waterstof kan ontbranden, wat leidt tot explosies.
* reactie met vocht: Zelfs het vocht in de lucht kan ervoor zorgen dat alkali -metalen reageren, dus het is cruciaal om ze droog te houden.
kerosine als oplossing:
* inert: Kerosine is een inerte koolwaterstof die niet reageert met alkali -metalen.
* Dichtheid: Kerosine is dichter dan water, dus het vormt een beschermende laag bovenop de alkali -metalen, waardoor ze niet in contact komen met vocht.
* NIET-FALBABLE: Kerosine is een ontvlambare vloeistof, maar het heeft een hoger flitspunt dan alkali -metalen, wat betekent dat het minder waarschijnlijk zal ontsteken.
Daarom houdt het opslaan van alkali -metalen in kerosine ze weg van zuurstof, vocht en lucht, waardoor potentieel gevaarlijke reacties worden voorkomen.
Opmerking: Hoewel kerosine een veel voorkomende methode is voor het opslaan van alkali -metalen, worden ook andere inerte vloeistoffen zoals minerale olie gebruikt.
Hoofdlijnen
- Waarom zijn alle levende organismen gegroepeerd in classificatiesystemen?
- Wat zijn oorzaken van evolutie en diversiteitsorganismen?
- Waarom tonen alle organismen variatie?
- Is uitsterven ooit een goede zaak?
- Nieuwe technologie verandert de manier waarop eiwitten in individuele cellen worden bestudeerd
- Wat zit er in een naam? In sommige gevallen een langere levensduur
- Hoe menselijk is onafhankelijkheid op biotische componenten?
- Wat is het type allel dat alleen het fenotype van het homozygoot chromosoom beïnvloedt?
- De ontwerpprincipes van celcompartimenten blootleggen
- Remedie tegen superbacteriën gevonden in kraaiheide

- Meervoudig gedoteerde hiërarchische poreuze koolstoffen voor superieure opslag van zinkionen
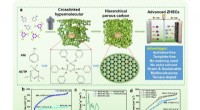
- Heterofase nanostructuren die bijdragen aan efficiënte katalyse
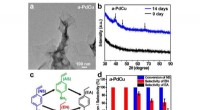
- Polymeermembranen kunnen baat hebben bij een duik

- Innovatieve verwerking en verpakking voor veilige, hoge kwaliteit, biologische bessenproducten

 Sedimentaire rotsen met rimpelmerken suggereren dat de gevormde waar?
Sedimentaire rotsen met rimpelmerken suggereren dat de gevormde waar?  Onderzoek heeft tot doel tweetalige leerders begrijpend lezen te stimuleren
Onderzoek heeft tot doel tweetalige leerders begrijpend lezen te stimuleren Biologie-experimenten van NASA zijn gebonden aan ruimtestations
Biologie-experimenten van NASA zijn gebonden aan ruimtestations Het ontwikkelen van een groot kooldioxide-omzettingssysteem, een kerntechnologie voor koolstofneutraliteit
Het ontwikkelen van een groot kooldioxide-omzettingssysteem, een kerntechnologie voor koolstofneutraliteit Wat is de atomiciteit van water?
Wat is de atomiciteit van water?  Een heliumtekort! Wat als we geen helium meer hebben?
Een heliumtekort! Wat als we geen helium meer hebben?  Er zijn hoge niveaus van PFAS-chemicaliën gevonden die in de rivier de Mersey stromen – nieuwe studie
Er zijn hoge niveaus van PFAS-chemicaliën gevonden die in de rivier de Mersey stromen – nieuwe studie  Bij welke soorten materialen is de kans het grootst dat er oxidatie optreedt?
Bij welke soorten materialen is de kans het grootst dat er oxidatie optreedt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


