
Wetenschap
Wat zijn meer reactieve alkali -metalen of alkline -aardmetalen?
* Elektronenconfiguratie: Alkali -metalen hebben één valentie -elektron in hun buitenste schaal, waardoor ze graag dat elektron willen verliezen om een stabiele edelgasconfiguratie te bereiken. Alkalische aardmetalen hebben twee valentie -elektronen.
* ionisatie -energie: Alkali -metalen hebben lagere ionisatie -energieën dan alkalische aardmetalen. Dit betekent dat er minder energie voor nodig is om een elektron uit een alkalimetaalatoom te verwijderen, waardoor ze eerder aan reacties deelnemen.
* elektropositiviteit: Alkali -metalen zijn elektropositiever (wat betekent dat ze de neiging hebben elektronen te verliezen) dan alkalische aardmetalen.
Samenvattend: Alkali -metalen zijn reactiever omdat ze gemakkelijker te ioniseren zijn en hun enkele valentie -elektron gemakkelijk verliezen om stabiele kationen te vormen.
Voorbeeld:
Natrium (NA), een alkalimetaal, reageert krachtig met water en produceert waterstofgas en natriumhydroxide. Calcium (CA), een alkalisch aardmetaal, reageert met water maar met een langzamere snelheid.
 Kun je wat grondstoffen bedenken die nodig zijn voor fotosynthese?
Kun je wat grondstoffen bedenken die nodig zijn voor fotosynthese?  Waarin verschilt een verbinding van een element?
Waarin verschilt een verbinding van een element?  Water vormt ruggengraat van hydratatie rond DNA, groepsvondsten
Water vormt ruggengraat van hydratatie rond DNA, groepsvondsten Twee hoofdelementen gevonden in het legeringsstaal?
Twee hoofdelementen gevonden in het legeringsstaal?  Onderzoek naar ontwikkelingen en uitdagingen op het gebied van elektrochemische nitraatreductie voor ammoniaksynthese
Onderzoek naar ontwikkelingen en uitdagingen op het gebied van elektrochemische nitraatreductie voor ammoniaksynthese
Hoofdlijnen
- Wat is een veronderstelde ontwikkeling van het leven van de gewone voorouder?
- Welke soorten moleculen katalyseren RNA-splitsing?
- Duivenvoetveergenen geïdentificeerd:onderzoek wijst uit hoe geschubde dinosauruspoten vogelachtige veren kunnen krijgen
- Hoe ras het luisteren tijdens politieke gesprekken beïnvloedt
- Wat leidt voedsel uit de bladeren tot wortels van de plant?
- Welke tak van wetenschapsiabetes hoort erbij?
- Uit welke componenten bestaat een ATP-molecuul?
- Welke klier produceert seratonine?
- Onderzoek identificeert mechanismen die bacteriële overleving bevorderen
- Problemen met bellen vermijden:onderzoek naar de relatie tussen bellen en elektrochemie

- Recente vorderingen in NMR-onderzoeken in vaste toestand van zeolietkatalysatoren

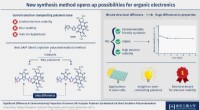
- Nieuwe synthesemethode opent mogelijkheden voor organische elektronica
- De moleculaire afbuiging van lichtstraling door middel van diamantaan

- Een vereenvoudigd nieuw proces zet houtafval uit landbouw en bosbeheer om in ethanol

 Een hoge concentratie van een mineraal in rots?
Een hoge concentratie van een mineraal in rots?  Is de studie van het universum genaamd astronomie of geologie oceanografie meteorologie?
Is de studie van het universum genaamd astronomie of geologie oceanografie meteorologie?  Kun je echt dubbelgebroken zijn?
Kun je echt dubbelgebroken zijn?  Kleine vulkanische meren die gigantische ondergrondse reservoirs aanboren
Kleine vulkanische meren die gigantische ondergrondse reservoirs aanboren Een oplaadbare nanozaklamp:Afterglow-luminescentiebeeldvorming volgt celgebaseerde microrobots in realtime
Een oplaadbare nanozaklamp:Afterglow-luminescentiebeeldvorming volgt celgebaseerde microrobots in realtime  nep nieuws, het eerste amendement en falen op de markt van ideeën
nep nieuws, het eerste amendement en falen op de markt van ideeën De vetten die in je lichaam zijn opgeslagen, bestaan meestal uit?
De vetten die in je lichaam zijn opgeslagen, bestaan meestal uit?  Uit het testen van de brieven van Vlad de Spietser blijkt dat hij mogelijk een aandoening heeft gehad waardoor zijn tranen met bloed vermengd waren
Uit het testen van de brieven van Vlad de Spietser blijkt dat hij mogelijk een aandoening heeft gehad waardoor zijn tranen met bloed vermengd waren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

