
Wetenschap
Wat gebeurt er als een zilveren lepel wordt bewaard in waterige oplossing van kopersulfaat?
1. Zilveren lepel wordt bruinrood:
* De zilveren lepel zal een roodbruine coating ontwikkelen terwijl koperen metaal op het oppervlak wordt afgezet. Dit komt omdat zilver reactiever is dan koper.
* De reactie is een enkele verplaatsingsreactie waarbij zilver (Ag) koper (Cu) verplaatst van de kopersulfaatoplossing.
2. Blauwe kleur van de oplossing vervaagt:
* De blauwe kleur van de kopersulfaatoplossing zal geleidelijk vervagen wanneer de koperionen (Cu²⁺) worden gereduceerd tot koperen metaal en afgezet op de zilveren lepel.
3. Vorming van zilverionen:
* Terwijl zilver koper in de oplossing vervangt, worden zilverionen (Ag⁺) in de oplossing vrijgegeven.
Hier is de chemische vergelijking die de reactie weergeeft:
`` `
2ag (s) + cuso₄ (aq) → cu (s) + ag₂so₄ (aq)
`` `
Verklaring:
* reactanten:
* Zilver (Ag) - de zilveren lepel
* Kopersulfaat (CUSO₄) - de waterige oplossing
* Producten:
* Koper (Cu) - Afgezet op de zilveren lepel
* Zilversulfaat (ag₂so₄) - opgelost in de oplossing
Samenvattend:
De zilveren lepel fungeert als een reductiemiddel, accepteert elektronen van koperionen en wordt bedekt met koperen metaal. De koperionen verliezen hun blauwe kleur als ze worden verminderd en de oplossing wordt minder blauw. Zilverionen worden in de oplossing vrijgegeven, waardoor een verandering in de samenstelling van de oplossing veroorzaakt.
 De structuur van een pathogeen effectoreiwit van Legionella pneumophila
De structuur van een pathogeen effectoreiwit van Legionella pneumophila Volledig inkjet-geprinte op vanadiumdioxide gebaseerde radiofrequentieschakelaars voor flexibele herconfigureerbare componenten
Volledig inkjet-geprinte op vanadiumdioxide gebaseerde radiofrequentieschakelaars voor flexibele herconfigureerbare componenten Is een vork een elementverbinding of mengsel?
Is een vork een elementverbinding of mengsel?  In welke stoffen zijn lignine en cellulose veranderd?
In welke stoffen zijn lignine en cellulose veranderd?  Welke ionische verbinding is Ca Br?
Welke ionische verbinding is Ca Br?
Hoofdlijnen
- Waarom is het logisch dat het laatste pad van aerobe ademhaling de meeste ATP afgeeft?
- Wat is de juiste definitie van een model in biologieverwaarden?
- Wat is de rol van dieren in de koolstofcyclus?
- De in 1995 opgegraven Plesiosaurus bleek een langnekkig zeereptiel te zijn
- Wat is het nucleïnezuur centraal in het metabolisme?
- 2 manieren waarop RNA is als DNA?
- Waarom vereist osmose een semipermeabiel membraan?
- Wat zijn chromosomen die vergelijkbare genetische informatie hebben genoemd?
- Wat zijn de vier categorieën van alle levende organismen?
- De studie van niet-covalente intermoleculaire interacties naar een nieuw gebied duwen
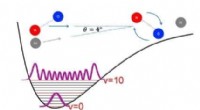
- De energieniveaus van organische halfgeleiders afstemmen

- Metaalfluisteren:een betere manier vinden om edele metalen uit elektronisch afval te halen
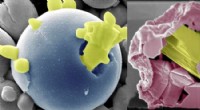
- Biosensor maakt realtime zuurstofmonitoring mogelijk voor organen-op-een-chip

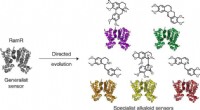
- Wetenschappers kapen bacteriën om de productie van medicijnen te vergemakkelijken
 Hoe bepaal je het atoomnummer van een atoom?
Hoe bepaal je het atoomnummer van een atoom?  Wat zijn de gevaren van het element helium?
Wat zijn de gevaren van het element helium?  Onderzoek naar dodelijke Italiaanse aardbevingen in 2016 kan toekomstige seismische voorspellingen verbeteren
Onderzoek naar dodelijke Italiaanse aardbevingen in 2016 kan toekomstige seismische voorspellingen verbeteren NASA ziet extra-tropische storm Saola langs Japan bewegen
NASA ziet extra-tropische storm Saola langs Japan bewegen Waarom wordt gammastraling gebruikt bij röntgenstraling?
Waarom wordt gammastraling gebruikt bij röntgenstraling?  Typen marine-patches voor beschadigde leidingen
Typen marine-patches voor beschadigde leidingen  Als het gaat om het uitstoten van elektronen, metaal glas verslaat plastic
Als het gaat om het uitstoten van elektronen, metaal glas verslaat plastic Wat zijn de oudste bomen in de wereld waarvan bekend is dat ze Northland zijn?
Wat zijn de oudste bomen in de wereld waarvan bekend is dat ze Northland zijn?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

