
Wetenschap
Wat gebeurt er met OH in een waterige oplossing wanneer H3O toeneemt?
Dit is waarom:
* KW is een constante: Het ionische product van water (KW) is een constante bij een gegeven temperatuur. Het vertegenwoordigt het product van de concentraties van H3O+ en OH-ionen in water. Bij 25 ° C, KW =1,0 x 10^-14.
* Inverse relatie: De vergelijking voor KW is:
KW =[H3O+] [OH-]
* verschuiving in evenwicht: Als de concentratie van H3O+ toeneemt, verschuift het evenwicht naar links om de constante waarde van KW te handhaven. Dit betekent dat de concentratie van OH- moet afnemen om de toename van H3O+te compenseren.
in eenvoudiger termen:
Stel je een wip. H3O+ en OH- staan aan tegenovergestelde uiteinden. Wanneer de ene kant omhoog gaat (H3O+ concentratie toeneemt), moet de andere kant naar beneden gaan (oh-concentratie neemt af) om de balans te handhaven (KW-constante).
Daarom leidt het verhogen van H3O+ in een waterige oplossing tot een afname van OH-concentratie. Dit maakt de oplossing meer zuur .
 Wie heeft het eerste scheikundelaboratorium uitgevonden?
Wie heeft het eerste scheikundelaboratorium uitgevonden?  Het toelaatbare concentratieniveau van vinylchloride C2H3CL In de atmosfeer is een chemische plant 1.8106 GL?
Het toelaatbare concentratieniveau van vinylchloride C2H3CL In de atmosfeer is een chemische plant 1.8106 GL?  Het smeltpunt van natriumbromide Een zout is 755c Bereken deze temperatuur in en f kelvins?
Het smeltpunt van natriumbromide Een zout is 755c Bereken deze temperatuur in en f kelvins?  Wat is de NH2 -functionele groep?
Wat is de NH2 -functionele groep?  Hoeveel elementen bestaan op natuurlijke wijze in vloeibare toestand?
Hoeveel elementen bestaan op natuurlijke wijze in vloeibare toestand?
 Hoe is de wetenschappelijke methode nuttig bij het oplossen van problemen buiten de wetenschap?
Hoe is de wetenschappelijke methode nuttig bij het oplossen van problemen buiten de wetenschap?  Episodische en intense regen veroorzaakt door de oude opwarming van de aarde
Episodische en intense regen veroorzaakt door de oude opwarming van de aarde Voordelen en nadelen van het wonen in de buurt van een bos?
Voordelen en nadelen van het wonen in de buurt van een bos?  Hoe helpen de bloemenbladeren en stengels planten om aan hun basisbehoeften te voldoen?
Hoe helpen de bloemenbladeren en stengels planten om aan hun basisbehoeften te voldoen?  Eetbare paddestoelen die op boomschors groeien
Eetbare paddestoelen die op boomschors groeien
Hoofdlijnen
- Interacties tussen eenvoudige moleculaire mechanismen leiden tot complexe infectiedynamiek
- De meeste hondensnoepjes overschrijden de aanbevolen dagelijkse hoeveelheid energie
- Welke levende wezens zijn volledig samengesteld uit een cel?
- Hoe wordt een vergrote en voedselopslag ondergrondse stengel genoemd?
- Wat zijn zeven verschillende soorten wetenschappers?
- Wat kunnen onderzoekers leren door vissen af te luisteren?
- Wat is het nut van chloroform in DNA -extractie uit organismen?
- Ultraconserverde elementen in het genoom:zijn ze onmisbaar?
- Hoe een zieke cel te resetten
- Toekomstige opties voor het opslaan van koolstofdioxide:Synthese van anorganische heteroalkenen
- Onderzoekers lossen controverse op over energiekloof van Van der Waals-materiaal

- Snelle test vindt tekenen van sepsis in een enkele druppel bloed

- Meervoudig mierachtig transport van neuronale lading door motoreiwitten

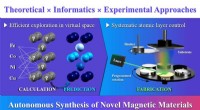
- Naar autonome voorspelling en synthese van nieuwe magnetische materialen
 Hoe komt zuurstof in een brandstofcel?
Hoe komt zuurstof in een brandstofcel? Wat zijn de onderdelen voor een atoom?
Wat zijn de onderdelen voor een atoom?  Coronavirus-tracking-app die privacy voorop stelt
Coronavirus-tracking-app die privacy voorop stelt NASA-NOAA-satelliet vangt tropische cycloon Blake en branden in West-Australië
NASA-NOAA-satelliet vangt tropische cycloon Blake en branden in West-Australië Studie stelt slimme hechtingen voor met sensoren voor wonden
Studie stelt slimme hechtingen voor met sensoren voor wonden Onderzoekers voeren uitgebreide studie uit van de samensmeltende melkwegcluster MACS J0417.5-1154
Onderzoekers voeren uitgebreide studie uit van de samensmeltende melkwegcluster MACS J0417.5-1154 Hoeveel mensen zijn er rond de maan gevlogen zonder te landen?
Hoeveel mensen zijn er rond de maan gevlogen zonder te landen?  Een nieuwe methode voor conforme afzetting van mangaanoxide op substraten met een hoge aspectverhouding
Een nieuwe methode voor conforme afzetting van mangaanoxide op substraten met een hoge aspectverhouding
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

