
Wetenschap
Wat is hetzelfde aan de elektronische structuur van lithium en natrium?
* Aantal valentie -elektronen: Zowel lithium als natrium hebben één valentie -elektron in hun buitenste schaal. Dit is het bepalende kenmerk van alkali -metalen en is verantwoordelijk voor hun vergelijkbare reactiviteit.
* Elektronenconfiguratie: Beide elementen hebben een enkel elektron in hun buitenste S-orbital.
* Lithium:1S² 2S¹
* Natrium:1S² 2S² 2P⁶ 3S¹
* Vergelijkbare reactiviteit: Vanwege hun enkele valentie -elektron verliezen beide elementen gemakkelijk dit elektron om een +1 kation te vormen, waardoor ze zeer reactief zijn. Deze reactiviteit wordt ook weerspiegeld in hun vergelijkbare chemische eigenschappen, zoals hun neiging om gewelddadig te reageren met water.
Het is echter belangrijk op te merken dat hun elektronische configuraties niet identiek zijn. Natrium heeft extra gevulde elektronenschalen in vergelijking met lithium, wat leidt tot een grotere atoomradius en een zwakkere aantrekkingskracht tussen de kern- en valentie -elektron. Dit verklaart de afnemende reactiviteit van alkali -metalen terwijl u de groep naar beneden gaat.
 Wetenschapsprojecten met neon en atomen
Wetenschapsprojecten met neon en atomen  Wat warmte ons kan vertellen over de chemie van batterijen:het Peltier-effect gebruiken om lithium-ioncellen te bestuderen
Wat warmte ons kan vertellen over de chemie van batterijen:het Peltier-effect gebruiken om lithium-ioncellen te bestuderen  Samen beter:Samengevoegde microscoop biedt ongekende kijk op biologische processen
Samen beter:Samengevoegde microscoop biedt ongekende kijk op biologische processen Wat zijn drie gebruik van waterstofgas?
Wat zijn drie gebruik van waterstofgas?  AI-simulatie van gearomatiseerde dampreacties onthult de vorming van veel gevaarlijke chemicaliën
AI-simulatie van gearomatiseerde dampreacties onthult de vorming van veel gevaarlijke chemicaliën
 Wat absorbeert de atmosfeer om de aarde te beschermen?
Wat absorbeert de atmosfeer om de aarde te beschermen?  Het verschil tussen boomsap en boomhars
Het verschil tussen boomsap en boomhars  Vervuiling door nutriënten maakt verzuring van de oceaan erger voor koraalriffen
Vervuiling door nutriënten maakt verzuring van de oceaan erger voor koraalriffen Klimaatwetenschappers zijn misschien niet de beste communicators van klimaatbedreigingen
Klimaatwetenschappers zijn misschien niet de beste communicators van klimaatbedreigingen De exodus van het Vanuatu-eiland gaat door, zelfs als de vulkaan zich stabiliseert
De exodus van het Vanuatu-eiland gaat door, zelfs als de vulkaan zich stabiliseert
Hoofdlijnen
- Hoe en waarom evolueerde homoseksueel gedrag bij mensen en andere dieren?
- Kunnen schimmels plastic vervangen?
- Een nieuwe ontdekking toont aan dat grote bloeiende planten 150 miljoen jaar ouder zijn dan eerder werd gedacht
- Eukaryotische cellen hebben lichamen die eiwitten en lipidenmoleculen in blaasjes wikkelen?
- Wat zijn de 4 belangrijkste elementen in organismen?
- Hoe reguleren planten hun suikermetabolisme?
- Wat zijn het soort fotosynthetische bacteriën?
- Hebben plantencellen nucleaire membranen?
- Zijn zoekmachines de filterbubbel aan het barsten? Uit onderzoek blijkt dat politieke ideologie een grotere rol speelt dan algoritmen
- Simulaties identificeren het belang van roostervervormingen in ionengeleidende brandstofcelmaterialen
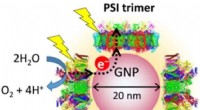
- Nieuw nano-apparaat zou zonne-energie kunnen gebruiken om waterstof te produceren
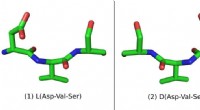
- Door de spiegel:nieuwe spiegelbeeldmoleculen kunnen leiden tot betere medicijnen
- Waterstof voedt raketten, maar hoe zit het met stroom voor het dagelijks leven? kwamen dichterbij

- Specifieke ioneneffecten gericht op aerogels van edelmetaal

 Wat is de chemische reactie wanneer gist in peroxide?
Wat is de chemische reactie wanneer gist in peroxide?  Wat zijn enkele landvormen in het noordoosten?
Wat zijn enkele landvormen in het noordoosten?  Een eierdruppelexperiment ontwerpen met behulp van rietjes
Een eierdruppelexperiment ontwerpen met behulp van rietjes Een zonne -flare is een soort van?
Een zonne -flare is een soort van?  Risicovrije gen-reactivering
Risicovrije gen-reactivering De evolutie van skyrmionen in Ir/Fe/Co/Pt-multilagen en hun topologische Hall-signatuur
De evolutie van skyrmionen in Ir/Fe/Co/Pt-multilagen en hun topologische Hall-signatuur Zal machine learning ons helpen buitenaards leven te vinden?
Zal machine learning ons helpen buitenaards leven te vinden?  Wat is een atoomscoop?
Wat is een atoomscoop?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

