
Wetenschap
Het molconcept is belangrijk in de chemie omdat?
1. Het bieden van een consistente eenheid voor het meten van materie:
- Het definieert een specifieke hoeveelheid materie, net zoals een dozijn 12 items vertegenwoordigt.
- Eén mol bevat altijd 6,022 x 10^23 deeltjes (atomen, moleculen, ionen, enz.), Zorg voor een gestandaardiseerde manier om hoeveelheden verschillende stoffen te vergelijken.
2. Massa, mol en aantal deeltjes met betrekking tot:
- De mol verbindt de macroscopische wereld (gram) met de microscopische wereld (atomen en moleculen).
- Met behulp van molaire massa (gram per mol) kunnen we eenvoudig omzetten tussen massa en mol, waardoor berekeningen mogelijk zijn met chemische reacties.
3. Stoichiometrie faciliteren:
- Chemische reacties treden op in specifieke molverhoudingen.
- Het molconcept stelt ons in staat om de hoeveelheden reactanten en producten die betrokken zijn bij een reactie te voorspellen, waardoor nauwkeurige berekeningen en voorspellingen mogelijk zijn.
4. Concentraties en oplossingen begrijpen:
- Molariteit (mollen per liter) is een belangrijke eenheid voor het uiten van de concentratie van oplossingen.
- Het begrijpen van mol molken maken nauwkeurige metingen en controle over chemische reacties in oplossingen mogelijk.
5. Atomaire massa's verbinden met praktische toepassingen:
- Het molconcept verbindt atomaire massa's (gebaseerd op koolstof-12) aan de massa's van stoffen die we in het laboratorium gebruiken.
- Dit stelt ons in staat om de massa's van specifieke chemicaliën te berekenen die nodig zijn voor experimenten of industriële processen.
In wezen dient het molconcept als een brug tussen de theoretische wereld van atomen en moleculen en de praktische wereld van chemische reacties en metingen. Het biedt een consistent en krachtig hulpmiddel voor het begrijpen en manipuleren van materie op zowel microscopisch als macroscopisch niveau.
 Waarom worden meer mensen waarschijnlijk getroffen als de chemische stof een gas is in plaats van vloeistof?
Waarom worden meer mensen waarschijnlijk getroffen als de chemische stof een gas is in plaats van vloeistof?  Wat is verzadigde oplossing eenvoudig definiëren?
Wat is verzadigde oplossing eenvoudig definiëren?  Elke stof die hydroxide-ionen in water vormt, kan een?
Elke stof die hydroxide-ionen in water vormt, kan een?  Hoeveel waterstofatomen worden aangetroffen in 2 moleculen hydroxylamine?
Hoeveel waterstofatomen worden aangetroffen in 2 moleculen hydroxylamine?  Gelijktijdige emissie van orthogonale handigheid in circulaire polarisatie
Gelijktijdige emissie van orthogonale handigheid in circulaire polarisatie
 NASA-waterdampbeelden tonen Tinos potentieel voor zware regen boven Fiji
NASA-waterdampbeelden tonen Tinos potentieel voor zware regen boven Fiji Hittegolf Zuid-Australië breekt recordtemperaturen
Hittegolf Zuid-Australië breekt recordtemperaturen Wereldwijde degradatie van land en natuur bedreigt welvaart en welzijn
Wereldwijde degradatie van land en natuur bedreigt welvaart en welzijn Soorten bomen in moerassen
Soorten bomen in moerassen Chinese satellieten bieden geavanceerde oplossingen voor het modelleren van kleine deeltjes
Chinese satellieten bieden geavanceerde oplossingen voor het modelleren van kleine deeltjes
Hoofdlijnen
- Welke organismen eten olie?
- Wat gebruikt Francium?
- Heeft uitwerpselen cellen erin?
- Wat is een zin die rijmt op bacteriën?
- De levenscyclus van een rozenplant
- Waarom evolutie van de mens beschouwd als een complex proces?
- Onderzoekers ontdekken nieuwe functie van oncoproteïnen
- Evolutiebiologen laten zien dat de kleurvarianten van vrouwelijke koekoeken gebaseerd zijn op oude mutaties
- Onderwaterkwekerijen helpen de mediterrane visbestanden nieuw leven in te blazen
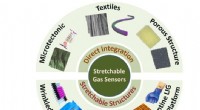
- Onderzoekers ontwikkelen sensoren die menselijke biomarkers en giftig gas detecteren
- Onderzoekers observeren direct de membraanbinding van α-synucleïne in levende cellen

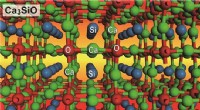
- Ontdekking van niet-toxische halfgeleiders met een directe band gap in het nabij-infrarood
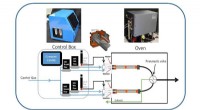
- Spoordampgenerator voor het opsporen van explosieven, verdovende middelen
- Lasers gebruiken om moleculaire mysteries in onze atmosfeer te visualiseren

 Hoe weten wetenschappers de structuur van het binnenste van de aarde?
Hoe weten wetenschappers de structuur van het binnenste van de aarde?  Groene watervoorziening en wereldwijde limieten
Groene watervoorziening en wereldwijde limieten Eerste Arabische set voor ISS zegt dat reis geschiedenis zal schrijven
Eerste Arabische set voor ISS zegt dat reis geschiedenis zal schrijven Consumer Electronics Show gaat voor spry-tech
Consumer Electronics Show gaat voor spry-tech  Nieuwe gevederde dinosaurus was een van de laatst overgebleven roofvogels
Nieuwe gevederde dinosaurus was een van de laatst overgebleven roofvogels Nieuw onderzoek laat zien hoe de persoonlijke omstandigheden van auteurs de weergave van de natuur in hun werken beïnvloeden
Nieuw onderzoek laat zien hoe de persoonlijke omstandigheden van auteurs de weergave van de natuur in hun werken beïnvloeden  Van welk element verwacht je dat het chemisch gedrag van Silicium het meest vergelijkbaar is?
Van welk element verwacht je dat het chemisch gedrag van Silicium het meest vergelijkbaar is?  Onderzoekers onthullen hoe de MRSA-bacterie omgaat met stress
Onderzoekers onthullen hoe de MRSA-bacterie omgaat met stress
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

