
Wetenschap
Welke veel voorkomende ionen worden meestal aangetroffen in zuren en basen?
zuren
* waterstofion (H+) :Dit is het bepalende kenmerk van een zuur. Zuren doneren waterstofionen in oplossing.
* Gemeenschappelijke anionen :
* haliden (Cl-, br-, i-) :Gevonden in zoutzuur (HCL), hydrobromzuur (HBR) en hydroiodinezuur (HI).
* nitraat (No3-) :Gevonden in salpeterzuur (HNO3).
* sulfaat (SO4^2-) :Gevonden in zwavelzuur (H2SO4).
* fosfaat (PO4^3-) :Gevonden in fosforzuur (H3PO4).
* carbonaat (co3^2-) :Gevonden in carbonzuur (H2CO3).
Bases
* Hydroxide-ion (OH-) :Dit is het bepalende kenmerk van een basis. Bases produceren hydroxide -ionen in oplossing.
* Gemeenschappelijke kationen :
* Alkali -metalen (Li+, Na+, K+, Rb+, Cs+) :Deze vormen sterke basen zoals lithiumhydroxide (LIOH), natriumhydroxide (NaOH), kaliumhydroxide (KOH), enz.
* Alkalische aardmetalen (Ca^2+, Sr^2+, ba^2+) :Deze vormen sterke bases zoals calciumhydroxide (Ca (OH) 2).
belangrijke opmerkingen:
* sterkte versus concentratie :Het is cruciaal om onderscheid te maken tussen zuur/base *sterkte *en *concentratie *.
* Kracht Verwijst naar hoe gemakkelijk een substantie protonen (H+ ionen) schenkt of accepteert. Sterke zuren/basen ioniseren volledig in oplossing.
* concentratie Verwijst naar de hoeveelheid zuur/base opgelost in een gegeven volume oplossing.
* Andere belangrijke ionen :Hoewel de hierboven genoemde ionen de meest voorkomende zijn, zijn er andere ionen die kunnen worden betrokken bij zuurbasischemie, zoals het ammoniumion (NH4+).
Laat het me weten als je nog andere vragen hebt!
 Staan er meer niet-metalen dan metalen in het periodiek systeem?
Staan er meer niet-metalen dan metalen in het periodiek systeem?  Hoe het aantal mollen in een oplossing te berekenen
Hoe het aantal mollen in een oplossing te berekenen  Onderzoekers beginnen inzicht te krijgen in de manier waarop giftige PFAS-chemicaliën zich verspreiden vanaf vrijgavelocaties
Onderzoekers beginnen inzicht te krijgen in de manier waarop giftige PFAS-chemicaliën zich verspreiden vanaf vrijgavelocaties  Zijn alle pigmenten gevonden in planten betrokken fotosynthese?
Zijn alle pigmenten gevonden in planten betrokken fotosynthese?  Wat zijn twee manieren om een oplossing te scheiden die vloeistoffen bevat?
Wat zijn twee manieren om een oplossing te scheiden die vloeistoffen bevat?
 Wat zijn de zeekoeienaanpassingen voor overleving?
Wat zijn de zeekoeienaanpassingen voor overleving?  De lichtheid of duisternis van kleur?
De lichtheid of duisternis van kleur?  Aziatische karpers die in veel grotere gebieden van Lake Michigan kunnen overleven dan eerder werd gedacht
Aziatische karpers die in veel grotere gebieden van Lake Michigan kunnen overleven dan eerder werd gedacht Hoe Wasops Nests Identificeren
Hoe Wasops Nests Identificeren  Fietspaden en voetpaden verminderen het autogebruik, uitstoot verminderen, studie vondsten
Fietspaden en voetpaden verminderen het autogebruik, uitstoot verminderen, studie vondsten
Hoofdlijnen
- Hoe de kaken van het leven werken
- Het andere pad van de keel leidt tot longen dat het wordt genoemd?
- Waarom worden chloroplasten als koolhydraatfabrieken en ribosomen beschouwd als eiwitfabrieken?
- Wat is de definitie van diafragma in samengestelde microscoop?
- Wat is aerobe fosforylering?
- Naburige celtypes beïnvloeden de variabiliteit van genexpressie in één cel
- Welke ketting is een volgorde van aminozuren die de basis voor basisstructuur -eiwit?
- Hebben dierencellen een kern die alle acties regelt?
- Hoe het genoom is verpakt in chromosomen die tijdens de celdeling getrouw kunnen worden verplaatst
- True to type:van menselijke biopsie tot complexe darmfysiologie op een chip
- Onderzoekers rapporteren nieuwe techniek voor het ontdooien van oppervlakken

- Licht ontspant kristal om de efficiëntie van zonnecellen te verhogen
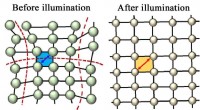
- Vloeistoffen tot het uiterste drijven met simulatiemethoden voor materialen van de volgende generatie
- Wetenschappers vinden handapparaat uit voor snelle bewaking van drinkwaterkwaliteit

 Dieren in de Middellandse Zee
Dieren in de Middellandse Zee  Op triazine gebaseerde, grafietkoolstofnitride als nieuwe tweedimensionale halfgeleider
Op triazine gebaseerde, grafietkoolstofnitride als nieuwe tweedimensionale halfgeleider Hoe science fiction recente hightech ontwikkelingen in de chemie voorspelde
Hoe science fiction recente hightech ontwikkelingen in de chemie voorspelde  Wat zijn tektonische platen geduwd?
Wat zijn tektonische platen geduwd?  Er moet rekening worden gehouden met zowel het potentieel als de beperkingen van herbebossing om de doelstellingen voor klimaatmitigatie te bereiken
Er moet rekening worden gehouden met zowel het potentieel als de beperkingen van herbebossing om de doelstellingen voor klimaatmitigatie te bereiken Nieuwe studie werpt licht op hoe intracellulaire pathogenen het immuunsysteem activeren
Nieuwe studie werpt licht op hoe intracellulaire pathogenen het immuunsysteem activeren  Hoe is het denatureren van een enzym onomkeerbaar?
Hoe is het denatureren van een enzym onomkeerbaar?  Wanneer kamer 70 graden Fahrenheit is, wat zou het dan op een Celsius -thermometer zijn?
Wanneer kamer 70 graden Fahrenheit is, wat zou het dan op een Celsius -thermometer zijn?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

