
Wetenschap
Wat zou er met druk gebeuren als het volume gas werd gehalveerd?
Dit betekent dat als u het volume van een gas halveert , de druk zal dubbel .
Hier is een eenvoudige uitleg:
* Stel je een vaste hoeveelheid gasmoleculen in een container voor.
* Wanneer u het volume vermindert (de container kleiner maakt), hebben de gasmoleculen minder ruimte om te bewegen.
* Dit betekent dat ze vaker botsen met de wanden van de container.
* Meer botsingen betekenen dat meer kracht op de muren wordt uitgeoefend, wat resulteert in een hogere druk.
formule:
De wet van Boyle kan wiskundig worden uitgedrukt als:
P₁v₁ =p₂v₂
Waar:
* P₁ =Initiële druk
* V₁ =eerste volume
* P₂ =uiteindelijke druk
* V₂ =definitief volume
In uw scenario, als v₂ =v₁/2, dan p₂ =2p₁.
 Is het onjuist dat de geur van een stof een voorbeeld van een fysieke eigenschap is?
Is het onjuist dat de geur van een stof een voorbeeld van een fysieke eigenschap is?  Wat is het verschil tussen organisch materiaal waaruit steenkool ontstaat en petroleum-aardgas voornamelijk?
Wat is het verschil tussen organisch materiaal waaruit steenkool ontstaat en petroleum-aardgas voornamelijk?  Wat zijn drie dingen waardoor schadelijke stoffen in de lucht terechtkomen?
Wat zijn drie dingen waardoor schadelijke stoffen in de lucht terechtkomen?  Hoge druk creëert nieuwe buren voor beryllium
Hoge druk creëert nieuwe buren voor beryllium Biosensor-chip detecteert draadloos single-nucleotide polymorfisme, met hogere gevoeligheid
Biosensor-chip detecteert draadloos single-nucleotide polymorfisme, met hogere gevoeligheid
 De handtekening van het Antropoceen op de berg Elbrus, Kaukasus
De handtekening van het Antropoceen op de berg Elbrus, Kaukasus Hoe snelwegbruggen zingen (of kreunen) in de regen om hun gezondheid te onthullen
Hoe snelwegbruggen zingen (of kreunen) in de regen om hun gezondheid te onthullen  Florida zet de standaard voor waterefficiëntie in het zuiden
Florida zet de standaard voor waterefficiëntie in het zuiden Bosbranden in Canada leiden tot luchtkwaliteitswaarschuwingen in de VS. Hier leest u hoe u veilig kunt blijven
Bosbranden in Canada leiden tot luchtkwaliteitswaarschuwingen in de VS. Hier leest u hoe u veilig kunt blijven  Basisinformatie over viskwekerijen
Basisinformatie over viskwekerijen
Hoofdlijnen
- Wat is het aantal kerncellen?
- Zijn fenotype en genotype -eigenschappen hetzelfde?
- Hoe zijn gymnospermen en angiospermen verschillend?
- Kan AI bedreigde mariene soorten helpen de klimaatverandering te overleven?
- Zijn essentiële aminozuren voor alle organismen?
- Welke van de volgende paden produceert de meeste NADH en de minste ATP?
- Bijen gebruiken patronen, niet alleen kleuren, om bloemen te vinden
- Gewone burgers helpen de wereldwijde dreiging van door muggen overgedragen ziekten te bestrijden
- Waar zijn bacteriofaag Lambda in?
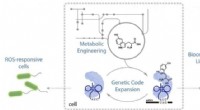
- Chemici breiden genetische code van E. coli uit om 21e aminozuur te produceren, het nieuwe vaardigheden geven
- Actie van geneesmiddelverbindingen in weefsel onthuld door nieuwe techniek
- Tetraëders kunnen de uniciteit van wateren verklaren

- Nieuwe katalysebenadering reduceert koolstofdioxide tot methaan

- Onderzoek naar perovskiet-silicium tandemcellen laat nieuwe weg zien

 De temperatuur van een gas is?
De temperatuur van een gas is?  Met een onverzadigbare vraag naar datacenters, sommigen zijn bezorgd dat Illinois het niet bij kan houden
Met een onverzadigbare vraag naar datacenters, sommigen zijn bezorgd dat Illinois het niet bij kan houden Wanneer is Haleys Comet in 2010?
Wanneer is Haleys Comet in 2010?  Onderzoekers bouwen robotwetenschapper die al een nieuwe katalysator heeft ontdekt
Onderzoekers bouwen robotwetenschapper die al een nieuwe katalysator heeft ontdekt Een ontwerpprincipe voor het creëren van selectieve en robuuste elektrokatalytische interfaces
Een ontwerpprincipe voor het creëren van selectieve en robuuste elektrokatalytische interfaces Wat als een asteroïde de aarde raakt?
Wat als een asteroïde de aarde raakt?  Magmakamers hebben een sponsachtige structuur
Magmakamers hebben een sponsachtige structuur Hoe is hydro -elektrisch vermogen slecht?
Hoe is hydro -elektrisch vermogen slecht?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

