
Wetenschap
Hoeveel keer geconcentreerd is de concentratie waterstofionen in een oplossing met pH van 3 dan die 5?
Inzicht in pH en waterstofionen
* pH: Een maat voor de zuurgraad of alkaliteit van een oplossing. Lagere pH -waarden duiden op een hogere zuurgraad (meer waterstofionen).
* waterstofionen (H+): Deze ionen zijn verantwoordelijk voor de zuurgraad van een oplossing.
De relatie
De pH -schaal is logaritmisch, wat betekent dat elke gehele getalverandering in pH een tienvoudig verschil in waterstofionconcentratie vertegenwoordigt.
Berekening
1. Verschil in pH: Het verschil in pH tussen 3 en 5 is 2.
2. concentratieverschil: Aangezien elk gehele getalverandering in pH een tienvoudig verschil is, betekent een verschil met 2 eenheden dat de oplossing met pH 3 100 keer is Meer geconcentreerd in waterstofionen dan de oplossing met pH 5 (10 x 10 =100).
Daarom is de waterstofionconcentratie in een oplossing met een pH van 3 100 keer hoger dan die van een oplossing met een pH van 5.
 Een 4 V-klasse metaalvrije organische lithium-ionbatterij komt dichter bij de realiteit
Een 4 V-klasse metaalvrije organische lithium-ionbatterij komt dichter bij de realiteit Hoe worden atomen bij elkaar gehouden in moleculen?
Hoe worden atomen bij elkaar gehouden in moleculen?  De weg vrijmaken voor kunstmatige fotosynthese:effect van doping op de fotokatalysator SrTiO3
De weg vrijmaken voor kunstmatige fotosynthese:effect van doping op de fotokatalysator SrTiO3 Kan ik melk in een hydrietoplossing mengen?
Kan ik melk in een hydrietoplossing mengen?  Geeft het aantal neutronen in de kern een atoom een unieke chemische aard?
Geeft het aantal neutronen in de kern een atoom een unieke chemische aard?
 Ballonmetingen onthullen eigenschappen van stofdeeltjes in de vrije troposfeer boven woestijn
Ballonmetingen onthullen eigenschappen van stofdeeltjes in de vrije troposfeer boven woestijn Vervuiling door bosbranden in Brazilië verslechtert de luchtkwaliteit in verre steden
Vervuiling door bosbranden in Brazilië verslechtert de luchtkwaliteit in verre steden De kosten verlagen van strategieën om de Overeenkomst van Parijs te bereiken
De kosten verlagen van strategieën om de Overeenkomst van Parijs te bereiken Professionele bemiddeling kan helpen bij het herstel van Everglades
Professionele bemiddeling kan helpen bij het herstel van Everglades Bossen vallen uiteen in de tropen, maar komen elders samen. Dit is wat het betekent voor dieren in het wild en het klimaat
Bossen vallen uiteen in de tropen, maar komen elders samen. Dit is wat het betekent voor dieren in het wild en het klimaat
Hoofdlijnen
- Is het levend of dood? Team laat zien hoe je de thermische handtekeningen van afzonderlijke cellen kunt meten
- Hoe de ‘loopbandband’ zorgt voor een goede celdeling
- De aandelen van Apple verzuren, die van Microsoft stijgen. Zeg wat?!
- Naar welke koninkrijken behoren bacteriën?
- Hoe wild is het Bengaalse kattengenoom?
- Hoe kleine chromosomen met grote concurreren om de aandacht van een cel
- Waarom zijn archaea en bacteriën anders dan andere koninkrijken?
- Wanneer is een stamcel echt een cel?
- Hoe wordt het organisme geclassificeerd?
- Apparaat verfijnt analyse van materialen voor brandstofcellen en batterijen

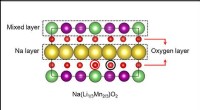
- Nieuw materiaal kan helpen de batterijkosten voor elektrische auto's te verlagen, telefoons
- Een nieuw potentieel alternatief voor muggenbestrijding ontdekt

- Comet inspireert chemie voor het maken van ademende zuurstof op Mars

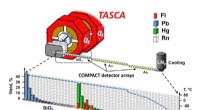
- Onderzoek toont aan dat flerovium het meest vluchtige metaal is in het periodiek systeem
 NASA's Mars 2020-rover wordt op de proef gesteld
NASA's Mars 2020-rover wordt op de proef gesteld Een ander Webb-telescoopinstrument maakt de weg vrij voor de wetenschap
Een ander Webb-telescoopinstrument maakt de weg vrij voor de wetenschap Computermodel voor het ontwerpen van eiwitsequenties die zijn geoptimaliseerd om te binden aan medicijndoelen
Computermodel voor het ontwerpen van eiwitsequenties die zijn geoptimaliseerd om te binden aan medicijndoelen Extreem lage thermische geleidbaarheid in 1-D zachte kettingstructuur
Extreem lage thermische geleidbaarheid in 1-D zachte kettingstructuur De voordelen van Open Pit Mining
De voordelen van Open Pit Mining Hoe gaan autistische personen om met het strafrechtsysteem?
Hoe gaan autistische personen om met het strafrechtsysteem? Wat heeft meer zetmeel een aardappel of een ui?
Wat heeft meer zetmeel een aardappel of een ui?  Lavastippen:wetenschappers maken holle, kwantumstippen met zachte schil
Lavastippen:wetenschappers maken holle, kwantumstippen met zachte schil
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

