
Wetenschap
Wat is de elektronenconfiguratie van MN in grondtoestand?
1S² 2S² 2P⁶ 3S² 3P⁶ 4S² 3D⁵
Hier is een uitsplitsing:
* 1S²: Het eerste energieniveau (n =1) heeft 2 elektronen in het orbitaal.
* 2s² 2p⁶: Het tweede energieniveau (n =2) heeft 2 elektronen in de s orbitale en 6 elektronen in het P -orbitaal.
* 3S² 3P⁶: Het derde energieniveau (n =3) heeft 2 elektronen in de s orbitale en 6 elektronen in het P -orbitaal.
* 4S² 3D⁵: Het vierde energieniveau (n =4) heeft 2 elektronen in het S -orbitaal en het 3D -orbitaal heeft 5 elektronen.
Belangrijke opmerking: Mogelijk ziet u de elektronenconfiguratie geschreven als [AR] 4S² 3D⁵ ook. Dit is een steno -notatie met behulp van het edelgasargon ([AR]) om de gevulde schelpen tot het 3P -orbitaal weer te geven.
 Wanneer u een metalen oppervlak beschrijft, welke en dan beschrijven de eigenschap?
Wanneer u een metalen oppervlak beschrijft, welke en dan beschrijven de eigenschap?  Wat is dodelijke fase en hoe wordt het berekend?
Wat is dodelijke fase en hoe wordt het berekend?  Hoe de paarse en roze zonnebrandmiddelen van rifkoralen werken
Hoe de paarse en roze zonnebrandmiddelen van rifkoralen werken  Wat is de reactie door suiker in een inerte atmosfeer te verwarmen?
Wat is de reactie door suiker in een inerte atmosfeer te verwarmen?  Wat is het mechanisme van vorming ftalisch anhydride?
Wat is het mechanisme van vorming ftalisch anhydride?
Hoofdlijnen
- Dankzij een krachtige nieuwe techniek kunnen wetenschappers bestuderen hoe eiwitten in cellen van vorm veranderen
- Nieuwe dataset werpt licht op de relatie tussen verrode zon-geïnduceerde chlorofylfluorescentie en fotosynthese op bladerdakniveau
- Is een eicelorgaan?
- Grizzlies keren terug naar de North Cascades in Washington. Hoe zal dat werken?
- Wat bedoelt hij in de wetenschapstermijn?
- Mosgenoomonderzoek identificeert twee nieuwe soorten
- Hoe verschillen in het genetische 'instructieboekje' tussen mensen en Neanderthalers eigenschappen beïnvloedden
- Hoe geven het overblijfselstructuren aan dat de huidige organismen verschillen van hun oude voorouders?
- Waarom is metafase belangrijk?
- Nieuwe inzichten in de vorming van metalen bulkglazen

- Wereldsnelheidsrecord voor polymeersimulaties meer dan honderdvoudig verbrijzeld

- Hogesnelheidsfilm helpt wetenschappers bij het ontwerpen van gloeiende moleculen

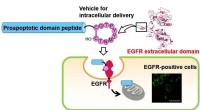
- Ontdekking van een nieuw voertuigpeptide opent een route voor medicijnafgifte
- Onderzoekers ontwikkelen op tillandsia geïnspireerde hygroscopische fotothermische organogels voor atmosferische waterwinning

 Hoe het creëren van minder gasachtige koeien de klimaatverandering kan helpen bestrijden
Hoe het creëren van minder gasachtige koeien de klimaatverandering kan helpen bestrijden  Welk sap zal het snelst verdampen met zout?
Welk sap zal het snelst verdampen met zout?  Kunnen we nog plezier hebben als het VK CO2-neutraal wordt?
Kunnen we nog plezier hebben als het VK CO2-neutraal wordt? Wearables en apparaten voor schimmels:biomaterialen maken de weg vrij voor de toekomst van sciencefiction
Wearables en apparaten voor schimmels:biomaterialen maken de weg vrij voor de toekomst van sciencefiction Kopen consumenten interessante producten met krediet en saai contant geld?
Kopen consumenten interessante producten met krediet en saai contant geld?  Toekomstig draagbaar apparaat zou kunnen vertellen hoe we menselijke beweging mogelijk maken
Toekomstig draagbaar apparaat zou kunnen vertellen hoe we menselijke beweging mogelijk maken Hoe wordt een controle gebruikt in een experiment?
Hoe wordt een controle gebruikt in een experiment?  Waarom zou een golfbaan minder biodiversiteit hebben dan natuurlijk ecosysteem, hoe zou het lagere effect rondom ecosysteem kunnen beïnvloeden?
Waarom zou een golfbaan minder biodiversiteit hebben dan natuurlijk ecosysteem, hoe zou het lagere effect rondom ecosysteem kunnen beïnvloeden?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

