
Wetenschap
Welke niet -eiwitmoleculen die tijdelijk samenwerken met enzymen tijdens chemische reacties in cellen?
Hier is een uitsplitsing van de verschillende soorten cofactors:
* Co -enzymen: Dit zijn organische moleculen die vaak zijn afgeleid van vitamines. Ze nemen rechtstreeks deel aan de chemische reactie door elektronen of atomen te accepteren of te doneren. Voorbeelden zijn NAD+, FAD en Coenzyme A.
* metaalionen: Dit zijn anorganische ionen die vaak nodig zijn voor de katalytische activiteit van het enzym. Ze kunnen helpen de enzymstructuur te stabiliseren, deel te nemen aan elektronenoverdrachtsreacties of interageren met het substraat. Voorbeelden zijn magnesium (mg2+), zink (Zn2+) en ijzer (Fe2+).
Cofactoren zijn essentieel voor de functie van veel enzymen. Ze kunnen:
* binden aan de actieve plaats van het enzym: Dit helpt het substraat correct te positioneren voor katalyse.
* Deelnemen rechtstreeks aan de chemische reactie: Ze kunnen elektronen, atomen of functionele groepen accepteren of doneren.
* Stabiliseer de enzymstructuur: Dit is belangrijk voor het handhaven van de activiteit van het enzym.
Hier zijn enkele voorbeelden van enzymen die cofactors vereisen:
* hexokinase: Dit enzym vereist magnesiumionen (mg2+) om de fosforylering van glucose te katalyseren.
* alcoholdehydrogenase: Dit enzym vereist dat het co -enzym NAD+ de oxidatie van alcohol katalyseert.
* carboxylase: Dit enzym vereist dat het co -enzymbiotine de overdracht van koolstofdioxide katalyseert.
Samenvattend zijn cofactoren essentieel voor de functie van veel enzymen. Het zijn niet -eiwitmoleculen die tijdelijk aan enzymen binden tijdens chemische reacties, waardoor het reactieproces wordt vergemakkelijkt.
 Wat is de algehele lading van een heliumatoom met 2 protonen neutronen en elektronen?
Wat is de algehele lading van een heliumatoom met 2 protonen neutronen en elektronen?  Hoe te weten wanneer een titratie voltooid is
Hoe te weten wanneer een titratie voltooid is Hoe scheid je een mengsel door middel van verdamping?
Hoe scheid je een mengsel door middel van verdamping?  Interpretatie van waterhardheid op niveau?
Interpretatie van waterhardheid op niveau?  Hoe bereken je het soortelijk gewicht van natriumsilicaat bij verschillende temperaturen?
Hoe bereken je het soortelijk gewicht van natriumsilicaat bij verschillende temperaturen?
Hoofdlijnen
- Gekruiste (evolutionaire) signalen?
- Mestcellen geven chemicaliën vrij die bekend staan als wat?
- Waar bevindt het plasmamembraan zich van de Elodea -cel?
- Een verklaring van het skeletsysteem
- Hoe het bewustzijn bij dieren onderzocht zou kunnen worden
- Kunnen honden snel woorden leren?
- Wat bevat je botten die rode bloedcellen maakt?
- Wat beschrijft een cel van verwelkte plant?
- Welke planten moeten gezond groeien?
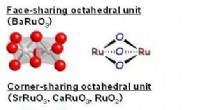
- Bariumruthenaat:een hoog rendement, gemakkelijk te hanteren perovskietkatalysator voor de oxidatie van sulfiden
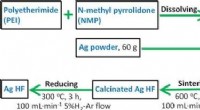
- Biodiesel gemaakt van afgedankte kartonnen dozen

- Onderzoekers stellen een nieuwe methode voor om de elektrokatalytische omzetting van koolstofdioxide te verbeteren
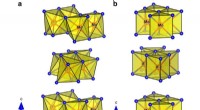
- Middelbare scholieren ontwikkelen een goedkoop filter om lood uit kraanwater te verwijderen

- Een nieuwe methode om waterstof efficiënter uit water te halen om duurzame energie op te vangen
 Wat is Bryophyllum kort uitgelegd?
Wat is Bryophyllum kort uitgelegd?  Satellietfoto's tonen gaten in ozonlaag?
Satellietfoto's tonen gaten in ozonlaag?  Kan een rekenmachine op zonne-energie werken?
Kan een rekenmachine op zonne-energie werken?  Te veel bankfusies kunnen kleine bedrijven schaden
Te veel bankfusies kunnen kleine bedrijven schaden Dieren van het bamboebos
Dieren van het bamboebos  Positieve effecten op het milieu door groen te worden
Positieve effecten op het milieu door groen te worden IJsbindende moleculen stoppen ijsgroei, fungeren als natuurlijke antivries
IJsbindende moleculen stoppen ijsgroei, fungeren als natuurlijke antivries Waarom wordt germanium niet gebruikt als LED-materiaal?
Waarom wordt germanium niet gebruikt als LED-materiaal?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

