
Wetenschap
Wat de vergelijkingsreactie tussen ijzer 3 chloride en ammoniumthiocyanaat?
Hier is de evenwichtige chemische vergelijking:
fecl₃ (aq) + 3nh₄scn (aq) ⇌ [fe (scn) ₃] ²⁻ (aq) + 3nh₄cl (aq)
Verklaring:
* reactanten:
* IJzer (III) chloride (Fecl₃) is een lichtgele oplossing.
* Ammoniumthiocyanaat (NH₄SCN) is een kleurloze oplossing.
* Producten:
* [Fe (scn) ₃] ²⁻: Dit is het ijzer (III) thiocyanaatcomplex ion, dat een diepe bloedrode oplossing vormt. Deze complexe formatie is de drijvende kracht van de reactie.
* Ammoniumchloride (NH₄CL) blijft in oplossing en is kleurloos.
Sleutelpunten:
* De reactie is omkeerbaar, wat betekent dat de producten kunnen reageren om opnieuw de reactanten te vormen. Dit wordt aangegeven door de dubbele pijl (⇌).
* De reactie wordt begunstigd in de voorwaartse richting, wat betekent dat de vorming van de rode complex ion waarschijnlijker is. Dit komt omdat de complexe ion zeer stabiel is.
* De kleurverandering van lichtgeel naar bloedrode is een visuele indicatie van de reactie die plaatsvindt.
Toepassingen:
Deze reactie heeft verschillende toepassingen, waaronder:
* chemische analyse: De intensiteit van de rode kleur kan worden gebruikt om de concentratie van ijzerionen in een oplossing te bepalen.
* Demonstraties: Het is een veel voorkomende demonstratie in chemieklassen om de concepten van evenwicht, complex ionenvorming en kleurverandering te illustreren.
 NASA vangt pasgeboren tropische cycloon Owens regenval, waargenomen door GPM-satelliet
NASA vangt pasgeboren tropische cycloon Owens regenval, waargenomen door GPM-satelliet Californië bestrijdt vuur met vuur om gigantische sequoia's te beschermen
Californië bestrijdt vuur met vuur om gigantische sequoia's te beschermen Wild-dweilingen identificeren
Wild-dweilingen identificeren De neerslag van lood door de brand in de Notre Dame werd waarschijnlijk over het hoofd gezien
De neerslag van lood door de brand in de Notre Dame werd waarschijnlijk over het hoofd gezien NASA ziet tropische depressie 9 ten oosten van Kleine Antillen
NASA ziet tropische depressie 9 ten oosten van Kleine Antillen
Hoofdlijnen
- Wat zijn kenmerken van de domein archaea en diverse informatie over dit domein?
- Hoe soorten ontstaan:wat de verwarde geschiedenis van de relaties tussen ijsberen en bruine beren ons vertelt
- Is T4 -bacteriofaag een DNA- of RNA -virus?
- Welk proces brengen organismen kooldioxide terug naar de atmosfeer?
- Wetenschappers bieden nieuw inzicht in de manier waarop bacteriën resistentiegenen tegen geneesmiddelen delen
- Onderzoekers concentreren zich op de manier waarop bacteriën voedselvergiftiging veroorzaken
- De meeste soorten, inclusief mensen, die in hun vroege levensjaren tegenslagen ervaren, lijden als volwassenen. Waarin verschillen gorilla's?
- Waarom likken en kauwen katten kattenkruid? Onderzoekers vinden een antwoord
- Mechanische eigenschappen van stamcellen kunnen voorspellen wat ze zullen worden
- Nog een reden om van de gestreepte bas te houden:antimicrobiële middelen

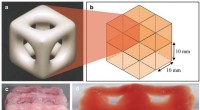
- 3D-printen creëert superzachte structuren die hersenen en longen nabootsen
- Onderzoek doen:ladingsstroom door eiwitten onderzoeken

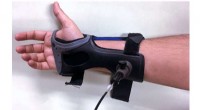
- Onderzoekers tonen effectiviteit nieuwe niet-invasieve bloedglucosetest aan
- Radiale synthese is baanbrekend voor chemisch onderzoek en productie

 Wat zijn specifieke biotechnologietoepassingen voor DNA-vingerafdrukken?
Wat zijn specifieke biotechnologietoepassingen voor DNA-vingerafdrukken?  Hoe verandert metamorfe rots naar sediment?
Hoe verandert metamorfe rots naar sediment?  Hoe een digitale schuifmaat te kalibreren
Hoe een digitale schuifmaat te kalibreren  Doorbraak in de nanowetenschap:deeltjes kleiner dan een miljardste meter onderzoeken
Doorbraak in de nanowetenschap:deeltjes kleiner dan een miljardste meter onderzoeken Wetenschappers bestuderen hoe een diabetesmedicijn de bodem beïnvloedt
Wetenschappers bestuderen hoe een diabetesmedicijn de bodem beïnvloedt  Het coronavirus kan Amerikaanse scholen dwingen om online les te geven. Zijn ze klaar?
Het coronavirus kan Amerikaanse scholen dwingen om online les te geven. Zijn ze klaar?  Stil stoppen? Als je verrast bent door de Amerikaanse anti-werkbeweging, moet je misschien meer films kijken
Stil stoppen? Als je verrast bent door de Amerikaanse anti-werkbeweging, moet je misschien meer films kijken Gekoelde elektriciteit
Gekoelde elektriciteit
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

