
Wetenschap
Wat is het verschil tussen nitriet en nitraation?
nitrite -ion (geen 2
* formule: Nee 2
* Oxidatietoestand van stikstof: +3
* Structuur: Gebogen, met een centraal stikstofatoom gebonden aan twee zuurstofatomen.
* eigenschappen:
* kleurloos: In verdunde oplossingen. Geconcentreerde oplossingen kunnen een lichtgele kleur hebben.
* Reducerend agent: Doneert gemakkelijk elektronen.
* giftig: Kan reageren met hemoglobine om methemoglobine te vormen, dat geen zuurstof kan dragen.
* conserveermiddel: Gebruikt in verwerkt vlees om bacteriegroei te voorkomen.
nitraation (geen 3
* formule: Nee 3
* Oxidatietoestand van stikstof: +5
* Structuur: Trigonale vlakke, met een centraal stikstofatoom gebonden aan drie zuurstofatomen.
* eigenschappen:
* kleurloos: In verdunde oplossingen. Geconcentreerde oplossingen kunnen een lichtgele kleur hebben.
* oxidatiemiddel: Accepteert gemakkelijk elektronen.
* Plant Nutrient: Essentieel voor plantengroei, die stikstof biedt.
* Waterverontreiniging: Kan schadelijk zijn voor de menselijke gezondheid in hoge concentraties, met name voor zuigelingen.
Belangrijkste verschillen:
| Feature | Nitriet (geen 2
| ---------------- | --------------------------- | ------------------------------ |
| Formule | Nee 2
| Oxidatietoestand | +3 | +5 |
| Structuur | Gebogen | Trigonal Planar |
| Chemisch gedrag | Reducerende agent | Oxiderend middel |
| Toxiciteit | Meer giftig | Minder giftig |
| Toepassingen | Voedselconserveermiddel | Plant Nutrient |
Conversie:
Nitrietionen kunnen worden geoxideerd tot nitraationen en nitraten kunnen worden gereduceerd tot nitrieten, afhankelijk van de omstandigheden.
Samenvattend:
Nitriet- en nitraationen zijn vergelijkbaar in uiterlijk, maar hebben verschillende chemische eigenschappen als gevolg van de verschillende oxidatietoestanden van stikstof. Nitriet is een reductiemiddel en is giftiger, terwijl nitraat een oxidatiemiddel is en dient als een plantenvoedingsstof.
 Coronavirus is een wake-up call:onze oorlog met het milieu leidt tot pandemieën
Coronavirus is een wake-up call:onze oorlog met het milieu leidt tot pandemieën Wat veroorzaakt een regenschaduw?
Wat veroorzaakt een regenschaduw?  Is de aarde 84 miljoen jaar geleden op zijn kant gevallen?
Is de aarde 84 miljoen jaar geleden op zijn kant gevallen? Een sprong voorwaarts in het schatten van het waterverbruik van gewassen
Een sprong voorwaarts in het schatten van het waterverbruik van gewassen Wanneer een groep op natuurwandeling gaat en alle eetbare planten identificeert. Welk type gegevens is dit?
Wanneer een groep op natuurwandeling gaat en alle eetbare planten identificeert. Welk type gegevens is dit?
Hoofdlijnen
- Iets dat niet gerelateerd is aan de wetenschap?
- Wat is het belang van pH in de landbouw?
- Wat is Bryophyllum kort uitgelegd?
- Een gelei -achtig materiaal buiten de kern, maar in celmembraan wordt de?
- Waarom heeft het aërobe metabolisme een voordeel ten opzichte van het anaërobe metabolisme bij levende wezens?
- Hoe heet het als een stengel opgroeit?
- Wat is belangrijker wetenschap of dromen?
- Wat is de formule voor cellulaire ademhaling?
- Onderzoekers bestuderen hoe zingende vleermuizen communiceren
- Wetenschappers hebben nieuwe verbindingen ontdekt met herbicide potentieel van zeeschimmel

- Wetenschappers hebben een materiaal ontwikkeld voor het nieuwe type liquid crystal displays
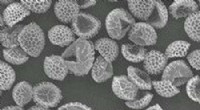
- Verontreinigende stoffen uit water verwijderen met stuifmeel en sporen - zonder de achoo!
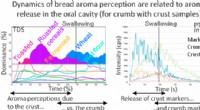
- Waarom een knapperige korst essentieel is voor het aroma en de smaak van baguettes
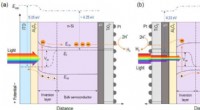
- Ruimtelijke ontkoppeling van lichtabsorptie- en reactieplaatsen in n-Si-fotokathoden voor het splitsen van zonnewater
 China's ZTE stopt met aandelenhandel na Amerikaans exportverbod
China's ZTE stopt met aandelenhandel na Amerikaans exportverbod De volgende maanlanding in de VS zal door particuliere bedrijven zijn, niet NASA
De volgende maanlanding in de VS zal door particuliere bedrijven zijn, niet NASA Er is meer transparantie nodig over de invloed van lobbyisten op Britse regelingen voor hernieuwbare energie
Er is meer transparantie nodig over de invloed van lobbyisten op Britse regelingen voor hernieuwbare energie Nanodeeltjes geassembleerd in tumoren vangen medicijnen en beeldvormende middelen op
Nanodeeltjes geassembleerd in tumoren vangen medicijnen en beeldvormende middelen op Wat kan gebruikt worden om een pH-waarde te verkrijgen?
Wat kan gebruikt worden om een pH-waarde te verkrijgen?  Kan suikermaïs worden verbouwd met minder atrazine?
Kan suikermaïs worden verbouwd met minder atrazine?  Welke mineralen en gesteenten worden in Turkije gevonden?
Welke mineralen en gesteenten worden in Turkije gevonden?  Zeer poreuze rotsen zijn verantwoordelijk voor het verrassend steile oppervlak van asteroïde Bennus
Zeer poreuze rotsen zijn verantwoordelijk voor het verrassend steile oppervlak van asteroïde Bennus
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

