
Wetenschap
Waarom heeft calciumcarbonaat een hoge temperatuur nodig om te ontleden?
* Sterke bindingen: De bindingen tussen calcium, koolstof en zuurstof in calciumcarbonaat zijn vrij sterk. Deze bindingen vereisen een aanzienlijke hoeveelheid energie om te breken.
* ontledingsproducten: De ontleding van calciumcarbonaat produceert calciumoxide (CaO) en koolstofdioxide (CO2). Dit is een chemische verandering waarbij het oorspronkelijke molecuul wordt onderverdeeld in eenvoudigere moleculen.
* Energie -input: De energie die nodig is om deze bindingen te verbreken, komt van warmte. Hoe hoger de temperatuur, hoe meer kinetische energie de moleculen hebben, waardoor de kans op binding vergroot.
Kortom, de hoge activeringsenergie die nodig is om de sterke bindingen in calciumcarbonaat te verbreken, vereist een hoge temperatuur om de ontledingsreactie te initiëren.
Hier is de reactie:
Caco3 (s) + warmte → Cao (s) + CO2 (g)
Opmerking: De ontleding van calciumcarbonaat is een omkeerbare reactie. Bij lagere temperaturen wordt de omgekeerde reactie (de reactie van calciumoxide met koolstofdioxide om calciumcarbonaat te vormen) de voorkeur.
 De weg verlichten naar poreuze elektronica en sensoren
De weg verlichten naar poreuze elektronica en sensoren Geminiaturiseerde lab-on-a-chip voor realtime chemische analyse van vloeistoffen
Geminiaturiseerde lab-on-a-chip voor realtime chemische analyse van vloeistoffen Hoeveel gram is 8 mol natriumchloride (NaCl)?
Hoeveel gram is 8 mol natriumchloride (NaCl)?  Verklaar de rol die opgeloste zuurstof speelt in het algemene mechanisme dat wordt voorgesteld om de verschillende stappen van spleetcorrosie te verklaren?
Verklaar de rol die opgeloste zuurstof speelt in het algemene mechanisme dat wordt voorgesteld om de verschillende stappen van spleetcorrosie te verklaren?  Welk element vertegenwoordigt een verbinding?
Welk element vertegenwoordigt een verbinding?
 Hoe beïnvloeden getijden activiteiten?
Hoe beïnvloeden getijden activiteiten?  De verwoestende regenval in India komt overeen met de voorspellingen voor klimaatverandering
De verwoestende regenval in India komt overeen met de voorspellingen voor klimaatverandering Waar wordt Nitrogyn in de natuur gevonden?
Waar wordt Nitrogyn in de natuur gevonden?  Wetenschappers detailleren onderzoek om de levensvatbaarheid en risico's van het ophelderen van mariene wolken te beoordelen
Wetenschappers detailleren onderzoek om de levensvatbaarheid en risico's van het ophelderen van mariene wolken te beoordelen  Hagedissen gevonden in Louisiana
Hagedissen gevonden in Louisiana
Hoofdlijnen
- Wetenschappers die onderzoek doen naar RNA-bewerking belichten mogelijke levensreddende behandelingen voor genetische ziekten
- Hoe worden enzymen beschadigd door hoge temperaturen?
- Definitie van menselijke biologie
- Verandering in de gencode kan verklaren hoe menselijke voorouders staarten verloren
- Nieuwe aanwijzingen waarom mutaties in het MYH9-gen een breed spectrum aan aandoeningen bij mensen veroorzaken
- Wat zijn belangrijkste landbouwproducten?
- Waarom evolutie sommige cellen tot altruïsme drijft
- Welke reproductie geeft planten meer variatie?
- Welke schadelijke effecten hebben sommige bacteriën op mensen?
- Langdurige geur is slechts een shampoo verwijderd, dankzij peptiden
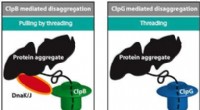
- Hoe ontvouwen cellulaire machines verkeerd gevouwen eiwitten?
- Onderzoekers gebruiken fotonen om metaalionen te scheiden

- Bomen en planten kunnen nieuwe toevoegingen worden in lichte voedingsproducten

- Baanbrekend onderzoek maakt kindervaccins veilig bij alle temperaturen

 Kaliumnitraatreactie-experimenten
Kaliumnitraatreactie-experimenten  Wat is kwantumknijpen?
Wat is kwantumknijpen?  Hersenorganoïden geven inzicht in de evolutie van het menselijk brein
Hersenorganoïden geven inzicht in de evolutie van het menselijk brein Lastige prestatie met opstaand molecuul
Lastige prestatie met opstaand molecuul Onderzoek onderzoekt hoe een sleutelgen het terpeenaroma in druiven moduleert
Onderzoek onderzoekt hoe een sleutelgen het terpeenaroma in druiven moduleert  Kleine sprinklerirrigatiemodellen voor schoolprojecten
Kleine sprinklerirrigatiemodellen voor schoolprojecten Welk experiment kunt u gebruiken om ijzeren aanmeldingen te scheiden van kleine stukjes lood?
Welk experiment kunt u gebruiken om ijzeren aanmeldingen te scheiden van kleine stukjes lood?  Zout helpt eiwitten om verder te komen
Zout helpt eiwitten om verder te komen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

