
Wetenschap
Wanneer de druk uitgeoefend op een beperkt gas bij constante temperatuur wordt verdubbeld volume is?
Wanneer de druk uitgeoefend op een beperkt gas bij constante temperatuur wordt verdubbeld, is het volume van het gas gehalveerd .
Dit is direct gerelateerd aan de wet van Boyle , die stelt:
* Voor een vaste hoeveelheid van een ideaal gas dat bij een constante temperatuur wordt bewaard, zijn druk en volume omgekeerd evenredig.
Wiskundig wordt dit weergegeven als:
* p₁v₁ =p₂v₂
Waar:
* P₁ =Initiële druk
* V₁ =eerste volume
* P₂ =uiteindelijke druk
* V₂ =definitief volume
Als u de druk verdubbelt (p₂ =2p₁), moet het volume worden gehalveerd (v₂ =v₁/2) om de vergelijking in balans te houden.
Hoofdlijnen
- Wat is de officiële naam van de kleinste en eenvoudigste cellen?
- Natuurlijke stoffen zijn veelbelovend tegen het coronavirus
- Wanneer u uw arm beweegt om computermuis te gebruiken, welke van deze spierceltypen is erbij betrokken?
- Supermensen creëren door middel van genmanipulatie en meer
- Waar is een pasgeboren baby -skelet van gemaakt?
- Wanneer water door een celmembraan beweegt, heet dit?
- Onderzoekers ontdekken hoe cysteïne een belangrijke regulator van de celgroei in gist activeert
- Wat ontwikkelt zich tijdens de celcyclus in een organisme?
- Wat zijn de natuurlijke hulpbronnen van haarlak?
- 3D-printen echt 3D maken

- Beton op basis van bacteriën biedt klimaatvoordelen

- Chemici synthetiseren een nieuwe katalysator voor olie- en gasverwerking
- een slimmere, veiligere manier om corrosie te verslaan:Onderzoek toont aan dat een nieuwe corrosieremmer 10 keer effectiever is

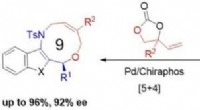
- Synthese van middelgrote ringstructuren
 Hoe heet de vloeistof in een thermometer?
Hoe heet de vloeistof in een thermometer?  Onderzoek leidt toekomst van plastic afval chemische recycling
Onderzoek leidt toekomst van plastic afval chemische recycling SNoOPI:een vliegende aas voor bodemvocht- en sneeuwmetingen
SNoOPI:een vliegende aas voor bodemvocht- en sneeuwmetingen Wat combineert om heliumatomen in een ster te vormen?
Wat combineert om heliumatomen in een ster te vormen?  Ontgrendel de kracht van bergkristal Betekenis:genezende eigenschappen en toepassingen
Ontgrendel de kracht van bergkristal Betekenis:genezende eigenschappen en toepassingen  Boornitride nanofilms voor bescherming tegen bacteriële en schimmelinfecties
Boornitride nanofilms voor bescherming tegen bacteriële en schimmelinfecties Wat staat bekend als het land tussen Twin Rivers?
Wat staat bekend als het land tussen Twin Rivers?  Nieuwe technologie zou de batterijwereld van kobalt kunnen ontdoen
Nieuwe technologie zou de batterijwereld van kobalt kunnen ontdoen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


