
Wetenschap
Wat gebeurt er in elektrochemische cel om ervoor te zorgen dat deze plat gaat?
1. Uitputting van reactanten:
* elektrochemische cellen werken door chemische energie om te zetten in elektrische energie. Dit proces omvat een chemische reactie tussen de reactanten bij de elektroden.
* Naarmate de reactie vordert, worden de reactanten geconsumeerd. Zie het als brandende brandstof in een auto - uiteindelijk raakt je geen benzine meer.
* Wanneer de reactanten zijn uitgeput, stopt de chemische reactie. Dit betekent dat de cel niet langer elektrische energie kan produceren en "gaat plat".
2. Evenwicht:
* elektrochemische reacties zijn omkeerbaar. Dit betekent dat de producten van de reactie ook kunnen reageren om de oorspronkelijke reactanten te vormen.
* Naarmate de reactie verloopt, neemt de concentratie van producten toe en neemt de concentratie reactanten af.
* Uiteindelijk wordt de snelheid van de voorwaartse reactie (reactanten op producten) gelijk aan de snelheid van de omgekeerde reactie (producten tot reactanten). Dit wordt evenwicht genoemd.
* Bij evenwicht is er geen netto verandering in de concentratie van reactanten of producten. Dit betekent dat de cel niet langer een potentieel verschil kan genereren en daarom geen stroom. De cel is effectief "plat" in deze toestand.
Andere factoren die kunnen bijdragen tot een plat die plat gaat:
* Interne weerstand: Na verloop van tijd kan de interne weerstand van de cel toenemen als gevolg van factoren zoals corrosie of opbouw van reactieproducten. Dit verhoogt het energieverlies in de cel, waardoor de output wordt verminderd.
* Temperatuur: Extreme temperaturen kunnen de snelheid van de chemische reactie en de prestaties van de cel beïnvloeden.
* lekkage: Als de cel beschadigd is of een defecte afdichting heeft, kan deze zijn elektrolytoplossing lekken, wat essentieel is voor de chemische reacties.
Samenvattend: Een elektrochemische cel "gaat plat" wanneer zijn reactanten zijn uitgeput of het evenwicht bereikt. Dit komt door de fundamentele principes van chemische reacties en de omzetting van chemische energie in elektrische energie.
 Wat is de kleinste staat in de VS? Kijkend naar oppervlakte en bevolking
Wat is de kleinste staat in de VS? Kijkend naar oppervlakte en bevolking  Super Typhoon Lekima-vaten richting China
Super Typhoon Lekima-vaten richting China Wat is het basispatroon van een chemische cyclus in een ecosysteem?
Wat is het basispatroon van een chemische cyclus in een ecosysteem?  Database van aardbevingen veroorzaakt door menselijke activiteit groeit - met enkele verrassingen
Database van aardbevingen veroorzaakt door menselijke activiteit groeit - met enkele verrassingen Captain Scotts Discovery-expeditie biedt 100 jaar later inzicht in klimaatverandering
Captain Scotts Discovery-expeditie biedt 100 jaar later inzicht in klimaatverandering
Hoofdlijnen
- Welke is een masterklier bij mensen?
- Zon, zee, duurzaamheid:zou je volgende Europese vakantie een groenere kunnen zijn?
- Welk water wordt getransporteerd van een wortels naar zijn bladeren in het weefsel?
- Wetenschappers gebruiken machine learning om antibioticaresistentie bij gekweekte kippen te bestrijden
- Het zit in de genen:onderzoek wijst uit hoe planten weten wanneer ze moeten bloeien
- Een ongewoon groot aantal uitgemergelde bruine pelikanen uit Californië komt aan land
- Aardworm Kenmerken
- Wat zijn de twee verschillende gezichten van fosfolipiden die een oppervlaktemembraan vormen, een cel?
- Wat wordt bedoeld met de alomtegenwoordigheid van micro -organismen?
- Technologie verhoogt de output van microfluïdische onderzoeksgegevens 100-voudig

- Nieuwe filtermethode belooft veiliger drinkwater, verbeterde industriële productie

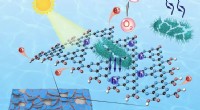
- Wetenschappers ontwikkelen metaalvrije fotokatalysator om pathogeenrijk water binnen enkele minuten te zuiveren
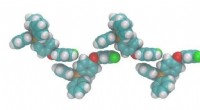
- Dankzij subtiele ioninteracties op moleculair niveau kunnen wetenschappers het smeltpunt van ionische verbindingen afstemmen
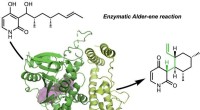
- Onderzoekers ontdekken eerste enzymen die een klassieke organische reactie katalyseren
 Londense rechtbank beslist of Uber moet blijven opereren
Londense rechtbank beslist of Uber moet blijven opereren Nieuw model voorspelt locaties van biologische hotspots in de oceaan
Nieuw model voorspelt locaties van biologische hotspots in de oceaan Welk type schaalkaart is geschaald op 175000?
Welk type schaalkaart is geschaald op 175000?  Hoe heeft de kosmische achtergrondstraling verhouden tot de vorming van het universum?
Hoe heeft de kosmische achtergrondstraling verhouden tot de vorming van het universum?  Hoe wordt Xenon-gas opgevangen?
Hoe wordt Xenon-gas opgevangen?  Wat gebeurt er als je zwavel en koper samen verwarmt?
Wat gebeurt er als je zwavel en koper samen verwarmt?  Qualcomm prijst 5G in 2019, lanceert nieuwe processor voor vlaggenschip smartphones
Qualcomm prijst 5G in 2019, lanceert nieuwe processor voor vlaggenschip smartphones Onderzoek onthult een dieper wordende watercrisis in Jordanië - en een weg voorwaarts
Onderzoek onthult een dieper wordende watercrisis in Jordanië - en een weg voorwaarts
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

