
Wetenschap
Hoeveel mol ionen worden vrijgegeven wanneer 42,1G CUSO4is opgelost in water?
1. Bereken de molaire massa van Cuso₄:
* Cu:63,55 g/mol
* S:32.06 g/mol
* O (4 atomen):16,00 g/mol x 4 =64,00 g/mol
* Totale molaire massa van CUSO₄ =63.55 + 32.06 + 64.00 =159,61 g/mol
2. Bereken de mol Cuso₄:
* Mol =massa / molaire massa
* Mol cuso₄ =42,1 g / 159,61 g / mol =0,264 mol
3. Bepaal de geproduceerde ionen:
* Wanneer Cuso₄ oplost in water, dissocieert het in koper (II) ionen (Cu²⁺) en sulfaationen (So₄²⁻):
* CUSO₄ (aq) → cu²⁺ (aq) + so₄²⁻ (aq)
4. Bereken de mol ionen:
* Aangezien een mol Cuso₄ één mol Cu²⁺ en één mol van SO₄²⁻ produceert, is het totale aantal mol ionen:
* 0,264 mol Cu²⁺ + 0,264 mol So₄²⁻ =0,528 mol ionen
Daarom komt 42,1 g Cuso₄ opgelost in water 0,528 mol ionen af.
 Welk van de elementen in het periodiek systeem heeft eigenschappen die het meest op fluor lijken?
Welk van de elementen in het periodiek systeem heeft eigenschappen die het meest op fluor lijken?  Wat vertegenwoordigt een mol van een stof op microscopische atoombasis?
Wat vertegenwoordigt een mol van een stof op microscopische atoombasis?  Waarom worden estersverbindingen ook derivaten van carbonzuur genoemd?
Waarom worden estersverbindingen ook derivaten van carbonzuur genoemd?  Kunstmatige chemicus combineert AI, robotica om autonome R&D uit te voeren
Kunstmatige chemicus combineert AI, robotica om autonome R&D uit te voeren Succesvolle toepassing van machine learning bij de ontdekking van nieuwe polymeren
Succesvolle toepassing van machine learning bij de ontdekking van nieuwe polymeren
 Waarom water centraal moet staan in klimaatactie
Waarom water centraal moet staan in klimaatactie  Hoe de hulpverlening bij rampen kan worden verbeterd met speltheorie
Hoe de hulpverlening bij rampen kan worden verbeterd met speltheorie NASA analyseerde de kracht van de tropische storm Fernands vóór de aanlanding
NASA analyseerde de kracht van de tropische storm Fernands vóór de aanlanding Regeling voor duurzame gecertificeerde palmolie haalt doelen niet
Regeling voor duurzame gecertificeerde palmolie haalt doelen niet IJzertekort beperkt mariene microben
IJzertekort beperkt mariene microben
Hoofdlijnen
- Hoe orang -oetans zich voortplanten?
- Welke erfenisfactoren beïnvloeden de metabolische snelheid?
- Wat zijn protozoën die niet kunnen worden geroepen?
- Juice:Waarom duurt het zo lang?
- Hoe peulvruchten zuurstof geven aan symbiotische bacteriën in hun wortels
- Voor fotosynthese heeft een cel wat 3 dingen nodig?
- Welke celorganel zit vol met waterig sap Welke twee functies voert het uit?
- Het oudste DNA ter wereld laat zien hoe mammoeten evolueerden
- Hoe voorspelbaar is evolutie?
- Het is een kwestie van hellingen

- Zuiver water uit de lucht halen, geïnspireerd door het leven in de woestijn

- Crowdfunding van een consumeerbare bolvormige waterfles - de Ooho!

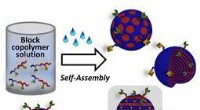
- Creatie en selectieve functionalisering van virusachtige polymeerdeeltjes
- Nieuwe tool verandert het spel voor heterogene materiaalmodellering

 Griekse dorpen geëvacueerd vanwege bosbrand
Griekse dorpen geëvacueerd vanwege bosbrand Video:SOHO's zicht op de zonnestorm van 11 mei 2024
Video:SOHO's zicht op de zonnestorm van 11 mei 2024  Nieuwe tool is bedoeld om COVID-19 te bestrijden, andere ziekten
Nieuwe tool is bedoeld om COVID-19 te bestrijden, andere ziekten Ontwikkeling van zeer gevoelige diode, zet microgolven om in elektriciteit
Ontwikkeling van zeer gevoelige diode, zet microgolven om in elektriciteit Hoe beïnvloedt de toevoeging van thermische energie de beweging van deeltjes?
Hoe beïnvloedt de toevoeging van thermische energie de beweging van deeltjes?  Potentieel alternatief voor petroleumpolycarbonaat dat bronnen van omgevingshormonen bevat
Potentieel alternatief voor petroleumpolycarbonaat dat bronnen van omgevingshormonen bevat Verweringspercentages voor gedolven land exponentieel hoger dan niet-gemijnde sites
Verweringspercentages voor gedolven land exponentieel hoger dan niet-gemijnde sites Hoe planten dieren naar het land dreven
Hoe planten dieren naar het land dreven
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

