
Wetenschap
Waarom wordt dampdruk verminderd in een oplossing met niet -vluchtige opgeloste stof?
1. Wat is dampdruk?
* Dampdruk is de druk die wordt uitgeoefend door de damp van een vloeistof wanneer deze in evenwicht is met zijn vloeibare fase. In eenvoudiger termen is het een maat voor hoeveel van de vloeistof wil ontsnappen in de gasfase.
2. Niet -vluchtige opgeloste stoffen
* Een niet -vluchtige opgeloste stof is een stof die niet gemakkelijk verdampt. Het heeft een zeer lage dampdruk in vergelijking met het oplosmiddel.
3. Het effect van de opgeloste stof
* Wanneer een niet -vluchtige opgeloste stof in een oplosmiddel wordt opgelost, verstoort deze de oplosmiddelmoleculen aan het oppervlak. De opgeloste moleculen bezetten ruimte aan het oppervlak, waardoor het moeilijker is voor de oplosmiddelmoleculen om in de gasfase te ontsnappen.
* Deze verstoring vermindert het aantal oplosmiddelmoleculen dat kan bijdragen aan de dampdruk.
4. Raoult's Law
* De wet van Raoult beschrijft dit fenomeen wiskundig. Het stelt dat de dampdruk van een oplossing gelijk is aan de molfractie van het oplosmiddel vermenigvuldigd met de dampdruk van het zuivere oplosmiddel:
* p oplossing =X oplosmiddel * P oplosmiddel
* Waar:
* P oplossing is de dampdruk van de oplossing
* X oplosmiddel is de molfractie van het oplosmiddel in de oplossing
* P oplosmiddel is de dampdruk van het pure oplosmiddel
* Sinds de molfractie van het oplosmiddel (x oplosmiddel ) is altijd minder dan 1 wanneer een opgeloste stof aanwezig is, de dampdruk van de oplossing (p oplossing ) zal lager zijn dan de dampdruk van het zuivere oplosmiddel (p oplosmiddel ).
Voorbeeld:
* Stel je voor dat je zout aan water toevoegt. Het zout verdampt niet, maar het neemt ruimte op aan het wateroppervlak. Dit maakt het moeilijker voor watermoleculen om in de lucht te ontsnappen, wat resulteert in een lagere dampdruk voor de zoutwateroplossing in vergelijking met zuiver water.
Samenvattend
De aanwezigheid van een niet -vluchtige opgeloste stof vermindert de dampdruk van een oplossing omdat deze oplosmiddelmoleculen aan het oppervlak blokkeert, waardoor ze niet gemakkelijk in de gasfase kunnen ontsnappen. Dit effect is direct gerelateerd aan de concentratie van de opgeloste stof in de oplossing.
 Wat is de witte poederachtige substantie die achterblijft in de pan na het koken van pijlpuntbronwater?
Wat is de witte poederachtige substantie die achterblijft in de pan na het koken van pijlpuntbronwater?  Nieuwe katalysatoren voor betere brandstofcellen
Nieuwe katalysatoren voor betere brandstofcellen Betaalbare en mobiele zuivering van dialysewater
Betaalbare en mobiele zuivering van dialysewater Duurzame spuitbetonmix-ontwerpen voor tunnels met een langere levensduur
Duurzame spuitbetonmix-ontwerpen voor tunnels met een langere levensduur Welke mineraalgroep bevat verbindingen van zuurstof en een metaal?
Welke mineraalgroep bevat verbindingen van zuurstof en een metaal?
Hoofdlijnen
- Hoe een van de X-chromosomen in vrouwelijke embryonale stamcellen tot zwijgen wordt gebracht
- Studie identificeert knelpunten in vroege zeegrasgroei
- Waar is de locatie van alle nucleïnezuren?
- Hoe rondwormen beslissen dat de tijd rijp is om te groeien
- Wat componeert DNA?
- Wat is de classificatie van een Colorado -kever?
- Wat beschermt je lichaam?
- Onderzoeker stelt antwoord voor waarom grotdieren blind worden
- Hoe zijn termen genlocus en allel gerelateerd?
- Neutronentomografie:inzicht in het inwendige van tanden, wortel ballen, batterijen, en brandstofcellen

- Een op origami geïnspireerde medische patch voor het afdichten van inwendige verwondingen

- Collageen in kraakbeenweefsel gedraagt zich als vloeibare kristallen op een smartphonescherm
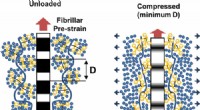
- Er gebeuren vreemde dingen als een kristal in tweeën wordt gesplitst

- Kleine hoeveelheden virus detecteren bij vroege infecties
 Welk woord betekent het gebruik van eenheden om een grootte -hoeveelheid te vinden?
Welk woord betekent het gebruik van eenheden om een grootte -hoeveelheid te vinden?  Ontdekking is de sleutel tot metaalslijtage in glijdende delen (met video)
Ontdekking is de sleutel tot metaalslijtage in glijdende delen (met video) Langetermijngegevens laten een recente versnelling zien in chemische en fysische veranderingen in de oceaan
Langetermijngegevens laten een recente versnelling zien in chemische en fysische veranderingen in de oceaan T. rex gebruikte een stijve schedel om zijn prooi op te eten
T. rex gebruikte een stijve schedel om zijn prooi op te eten De lancering van SpaceX vanavond zou de 300e boosterlanding markeren, indien succesvol
De lancering van SpaceX vanavond zou de 300e boosterlanding markeren, indien succesvol  Nano-elektromechanische resonatoren gebaseerd op superroosters van hafnia-zirkoniumoxide-aluminiumoxide met gigahertz-spectrumdekking
Nano-elektromechanische resonatoren gebaseerd op superroosters van hafnia-zirkoniumoxide-aluminiumoxide met gigahertz-spectrumdekking  Nieuw model laat zien hoe ineengedoken pinguïns de warmte eerlijk delen
Nieuw model laat zien hoe ineengedoken pinguïns de warmte eerlijk delen  Wat heeft meer atomen 2,88 gram helium of 16,4 zinkatomen?
Wat heeft meer atomen 2,88 gram helium of 16,4 zinkatomen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

