
Wetenschap
Wat reageert de term met zuurstof?
Hier is een uitsplitsing:
* Chemische verandering: De chemische samenstelling van de stof verandert en vormen nieuwe stoffen.
* zuurstof: Het zuurstofmolecuul (O2) is betrokken bij de chemische reactie.
* Vorming van nieuwe bindingen: De atomen van de stof- en zuurstofatomen herschikken zichzelf en vormen nieuwe bindingen.
* Energieafgifte of absorptie: Dit proces kan energie vrijgeven (exotherme reactie) of energie absorberen (endotherm reactie).
Gemeenschappelijke voorbeelden:
* verbranding: Het branden van hout, brandstof of andere materialen in aanwezigheid van zuurstof geeft warmte en licht vrij, wat resulteert in de vorming van koolstofdioxide en water.
* roesten: IJzer reageert met zuurstof en water om ijzeroxide (roest) te vormen, een proces dat het ijzer verzwakt.
* ademhaling: Levende organismen nemen zuurstof in en gebruiken het om voedselmoleculen af te breken, energie vrij te geven en koolstofdioxide en water te produceren.
Niet alle reacties met zuurstof zijn hetzelfde:
* oxidatie: Een brede term die elke reactie beschrijft waarin een stof elektronen verliest. Reacties met zuurstof zijn vaak oxidatiereacties, maar niet alle oxidatiereacties omvatten zuurstof.
* verbranding: Een specifiek type oxidatiereactie waarbij de snelle reactie van een stof met zuurstof wordt betrokken, waardoor warmte en licht produceren.
Over het algemeen betekent "reageert met zuurstof" een chemisch proces waarbij zuurstof betrokken is bij de vorming van nieuwe stoffen en de afgifte of absorptie van energie.
 Kan carbonzuur reageren met Grignard-reagens?
Kan carbonzuur reageren met Grignard-reagens?  Welk type atomen vormen doorgaans ionische of covalente bindingen?
Welk type atomen vormen doorgaans ionische of covalente bindingen?  Nieuwe materialen kunnen wondgenezing stimuleren door gebruik te maken van natuurlijke genezingsmethoden
Nieuwe materialen kunnen wondgenezing stimuleren door gebruik te maken van natuurlijke genezingsmethoden Hoe reageert kaliumjodiumoplossing met zetmeel?
Hoe reageert kaliumjodiumoplossing met zetmeel?  Het leven een nieuwe truc leren:bacteriën maken borium-koolstofbindingen
Het leven een nieuwe truc leren:bacteriën maken borium-koolstofbindingen
 Dit is wat u moet weten over het afvangen en opslaan van koolstof
Dit is wat u moet weten over het afvangen en opslaan van koolstof Studie volgt stormwater orkaan Harvey met GPS
Studie volgt stormwater orkaan Harvey met GPS Wat heeft een gebouw nodig om zichzelf ‘toegankelijk’ te noemen – en is dat voldoende?
Wat heeft een gebouw nodig om zichzelf ‘toegankelijk’ te noemen – en is dat voldoende?  Te warm voor comfort:de fysiologische gevaren van extreme hitte
Te warm voor comfort:de fysiologische gevaren van extreme hitte Arctische open water perioden zullen naar verwachting dramatisch verlengen tegen 2100
Arctische open water perioden zullen naar verwachting dramatisch verlengen tegen 2100
Hoofdlijnen
- Kikker en menselijke bloedcellen vergelijken en identificeren
- Hoe vakantiefoto's van zebra's en walvissen het behoud kunnen helpen
- Wat is het belangrijkste kenmerk van sponzen?
- Hoe bacteriën zich hechten aan vezels in de darmen
- Zijn kankersoorten nieuw ontwikkelde soorten?
- Welke machine maakt kleine voren en zaait zaden erin?
- Hoe cellen DNA-schadeherstelroutes selecteren
- Welk deel van de bacterie kan het beschermen tegen fagocytose door witte bloedcellen?
- Waar worden geslachtscellen bij mensen geproduceerd?
- Nieuw geavanceerd materiaal vertoont buitengewone stabiliteit over een breed temperatuurbereik

- Samenstellingsontwerp van legeringen met meerdere componenten door screening met hoge doorvoer

- Laser volgt therapieën, voedingsstoffen, gifstoffen

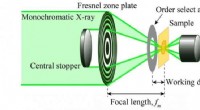
- Een scanning transmissie-röntgenmicroscoop voor analyse van chemische toestanden van lithium
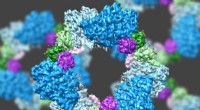
- Wetenschappers geven een glimp met hoge resolutie van de enzymstructuur
 Hillwood wil AllianceTexas veranderen in mobiliteitsinnovatiezone voor drones, autonome voertuigen
Hillwood wil AllianceTexas veranderen in mobiliteitsinnovatiezone voor drones, autonome voertuigen Coronavirus zorgt voor nieuwe hit in duizelingwekkende mediasector
Coronavirus zorgt voor nieuwe hit in duizelingwekkende mediasector Aan het ene uiteinde van een tRNA -molecuul bestaat er een korte staart. Deze staart?
Aan het ene uiteinde van een tRNA -molecuul bestaat er een korte staart. Deze staart?  Wat is een kwaadaardige tumor die zich ontwikkelde uit epitheelweefsel?
Wat is een kwaadaardige tumor die zich ontwikkelde uit epitheelweefsel?  Voor mensen die stotteren, het gemak van spraakassistenttechnologie blijft buiten bereik
Voor mensen die stotteren, het gemak van spraakassistenttechnologie blijft buiten bereik Hoe groot zijn de planeten vergeleken met de aarde?
Hoe groot zijn de planeten vergeleken met de aarde?  Digitale gegevens van bewaarde planten en dieren veranderen de manier waarop wetenschappers de wereld verkennen
Digitale gegevens van bewaarde planten en dieren veranderen de manier waarop wetenschappers de wereld verkennen  Wanneer twee continenalplaten uiteenlopen, welke landvormen worden gemaakt?
Wanneer twee continenalplaten uiteenlopen, welke landvormen worden gemaakt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

