
Wetenschap
Welke groep zal reageren met alkali -metalen om ionische bindingen te vormen?
Dit is waarom:
* Alkali -metalen: Deze zijn in groep 1 van de periodiek systeem en hebben één valentie -elektron. Ze zijn zeer reactief en hebben de neiging dit elektron te verliezen om een stabiel octet te bereiken.
* halogenen: Deze zijn in groep 17 van de periodiek systeem en hebben zeven valentie -elektronen. Ze zijn ook erg reactief en krijgen gemakkelijk één elektron om een stabiel octet te bereiken.
Wanneer een alkalimetaal en een halogeen reageren, verliest het alkali -metaalatoom zijn valentie -elektron om een positief geladen ion (kation) te vormen. Het halogeenatoom krijgt dit elektron om een negatief geladen ion (anion) te vormen. De tegenovergestelde ladingen trekken aan en vormen een ionische binding.
Voorbeeld: Natrium (NA) reageert met chloor (CL) om natriumchloride (NaCl) te vormen.
* Na verliest een elektron om Na+ te worden
* Cl krijgt een elektron om Cl- te worden
* De tegengesteld geladen ionen vormen vervolgens een ionische binding.
Laat het me weten als je meer voorbeelden wilt of andere soorten chemische reacties wilt verkennen!
 Loodbesmetting gevonden in melktanden van kinderen die in de buurt van Exide-batterijfabriek wonen
Loodbesmetting gevonden in melktanden van kinderen die in de buurt van Exide-batterijfabriek wonen Een glas whisky kan je helpen om diep in de tijd te komen
Een glas whisky kan je helpen om diep in de tijd te komen Hoe zit het met de recente wilde tornado's? Deskundige weegt mee
Hoe zit het met de recente wilde tornado's? Deskundige weegt mee  Australische onderzoekers laten de evolutie van de bloemkleur zien, aangedreven door de voorkeuren van bijen
Australische onderzoekers laten de evolutie van de bloemkleur zien, aangedreven door de voorkeuren van bijen  NASA's Aqua-satelliet volgt tropische cycloon Lorna
NASA's Aqua-satelliet volgt tropische cycloon Lorna
Hoofdlijnen
- Wat synthetiseert eiwitten?
- Het instinct voor vechten of vluchten is misschien veel ouder dan we dachten
- Nieuw inzicht in hoe planten cellulose maken
- geproduceerd door het lichaam om u te helpen beschermen tegen ziekten?
- Zit in de erwtenplanten Tall-STEM- en korte allel verschillende vormen van hetzelfde?
- Waar wordt Myelin gevonden en wat zijn functie?
- Er worden meer koeien getest en gevolgd op vogelgriep. Dit is wat dat betekent
- Wat is de wetenschappelijke naam voor PBO?
- Waar komen haarcellen daar nuritioment vandaan?
- High-tech detectie verlicht stresstesten voor beton

- Optische detectie van meerdere bacteriesoorten met behulp van metaal-organische hybriden op nanometerschaal

- Belangrijkste mechanismen van luchtwegontspanning bij astma onthuld in nieuwe studie
- Wat zeekomkommers ons kunnen leren over zelfverdediging

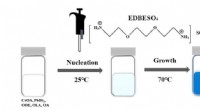
- Een nieuwe strategie om blauw licht te creëren uit een veelbelovend materiaal
 Virussen delen genen met organismen in de levensboom
Virussen delen genen met organismen in de levensboom Een nieuw venster op planten uit het verleden
Een nieuw venster op planten uit het verleden Studie biedt inzicht in hoe klimaatverandering de geografische verspreidingsgebieden van soorten kan beïnvloeden
Studie biedt inzicht in hoe klimaatverandering de geografische verspreidingsgebieden van soorten kan beïnvloeden  Studie werpt nieuw licht op hoe dieren en planten reageren op veranderingen in de omgeving
Studie werpt nieuw licht op hoe dieren en planten reageren op veranderingen in de omgeving Hoe rekbare vloeistoffen reageren op golvende oppervlakken
Hoe rekbare vloeistoffen reageren op golvende oppervlakken De top 10-onderwerpen voor onderzoeksdocumenten
De top 10-onderwerpen voor onderzoeksdocumenten  Waarom zijn overgangsmetalen goede katalysatoren?
Waarom zijn overgangsmetalen goede katalysatoren?  diamanten krijgen, temperatuur opnemen:Kwantumthermometer die nanodiamanten gebruikt, detecteert koorts in kleine wormen C. elegans
diamanten krijgen, temperatuur opnemen:Kwantumthermometer die nanodiamanten gebruikt, detecteert koorts in kleine wormen C. elegans
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

