
Wetenschap
Het monomeer dat verantwoordelijk is voor de vorming van sulfidebindingen in polypeptiden is?
Dit is waarom:
* sulfidebindingen (disulfidebindingen) worden niet gevormd door monomeren. Ze worden gevormd tussen de zwavelatomen van cysteïne -aminozuurresiduen . Cysteïne is een standaard aminozuur gevonden in eiwitten.
* monomeren zijn de individuele bouwstenen van grotere moleculen. In het geval van eiwitten zijn de monomeren aminozuren.
Hoe disulfidebindingen vormen:
1. Twee cysteïneresten Kom in de buurt in het gevouwen eiwit.
2. De zwavelatomen Op de cysteïneresten reageren en vormen een disulfidebinding .
3. Deze binding helpt de driedimensionale structuur van het eiwit te stabiliseren .
Samenvattend: Hoewel cysteïne het aminozuur is dat betrokken is bij de vorming van disulfidebindingen, is het geen monomeer dat direct de binding creëert. De binding zelf wordt gevormd door een reactie tussen de zwavelatomen van twee cysteïneresten in het eiwit.
 Wat voor soort landvormen creëren secundaire krachten?
Wat voor soort landvormen creëren secundaire krachten?  Welke dieren eten teken van herten?
Welke dieren eten teken van herten?  Studie vordert het begrijpen van de verhalen van het oude klimaat verteld door kleine schelpen
Studie vordert het begrijpen van de verhalen van het oude klimaat verteld door kleine schelpen De rommelende vulkaan Indonesië kan meer tsunami's veroorzaken, experts waarschuwen
De rommelende vulkaan Indonesië kan meer tsunami's veroorzaken, experts waarschuwen Zullen we ooit onze afhankelijkheid van buitenlandse olie verminderen?
Zullen we ooit onze afhankelijkheid van buitenlandse olie verminderen?
Hoofdlijnen
- Geboortebeperking voor parasieten:onderzoekers onthullen nieuw vaccindoelwit voor malaria
- Wat is een DNA gerelateerd aan Gene?
- Zouden mensen bereid zijn hun persoonsgegevens af te staan voor onderzoek?
- Hoe klonen werkt
- Voorbereid op oorlog:hoe cellen virale invasie overleven
- Onderzoekers laten zien hoe gifstoffen van de bacterie Clostridium difficile in de darmcellen terechtkomen
- Cassave beschermen tegen ziekten? Daar is een app voor
- Het niveau van eiwitstructuur dat de sequentie -aminozuren is?
- Welk deel van de cel creëert eiwitten voor cel?
- Atomaire vingerafdruk identificeert emissiebronnen van uranium

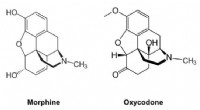
- Minder verslavende opioïden ontwerpen door middel van chemie
- Micro-organismen helpen bij de productie

- Een Rubiks microfluïdische kubus

- Softwareprogramma Allchemy identificeert prebiotische synthese van biochemische verbindingen uit oer-precursoren

 Welke elementen onder de norm voor gevarencommunicatie zijn vereist op elk etiket voor gevaarlijke chemische stoffen?
Welke elementen onder de norm voor gevarencommunicatie zijn vereist op elk etiket voor gevaarlijke chemische stoffen?  Waarom wordt de cyclus beschouwd als een aerobe proces?
Waarom wordt de cyclus beschouwd als een aerobe proces?  Nieuwe mechanismen ontdekt die bacteriën gebruiken om zichzelf te beschermen tegen antibiotica
Nieuwe mechanismen ontdekt die bacteriën gebruiken om zichzelf te beschermen tegen antibiotica Grafeen vertoont een uniek potentieel om de bandbreedtevereisten van toekomstige telecommunicatie te overtreffen
Grafeen vertoont een uniek potentieel om de bandbreedtevereisten van toekomstige telecommunicatie te overtreffen Onderzoekers observeren unieke tussenlaagtoestand in een dubbellaagse heterostructuur
Onderzoekers observeren unieke tussenlaagtoestand in een dubbellaagse heterostructuur Opgesloten lichtbanen binnen een intrigerend materiaal
Opgesloten lichtbanen binnen een intrigerend materiaal Groeien alle ware noten op bomen?
Groeien alle ware noten op bomen?  Dubbele ongelijkheden oplossen
Dubbele ongelijkheden oplossen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

