
Wetenschap
Wat is de edelgasconfiguratie van arseen?
1. Zoek het atoomnummer van Arseen:
Arseen heeft een atoomnummer van 33, wat betekent dat het 33 protonen en 33 elektronen heeft.
2. Identificeer het voorgaande edelgas:
Het edelgas dat vóór arseen op het periodiek systeem komt, is argon (AR), dat een atoomnummer van 18 heeft.
3. Schrijf de edelgaskern:
De edelgasconfiguratie van argon is [AR].
4. Bepaal de resterende elektronen:
Arseen heeft 33 elektronen en argon heeft 18 elektronen, waardoor 15 elektronen rekening houden (33 - 18 =15).
5. Vul de resterende orbitalen:
- De volgende orbital is de 4S orbital, die 2 elektronen kan bevatten:[AR] 4S²
- Dan is de 3D -orbital gevuld met 10 elektronen:[AR] 4S² 3D¹⁰
- Ten slotte ontvangt de 4P orbitaal de resterende 3 elektronen:[AR] 4S² 3D¹⁰ 4P³
Daarom is de edelgasconfiguratie van arseen [AR] 4S² 3D¹⁰ 4P³.
 Wat zijn de zes belangrijkste soorten ecosystemen?
Wat zijn de zes belangrijkste soorten ecosystemen?  De inspanningen van China om de luchtvervuiling in grote steden te verminderen, bleken de vervuiling in nabijgelegen gebieden te vergroten
De inspanningen van China om de luchtvervuiling in grote steden te verminderen, bleken de vervuiling in nabijgelegen gebieden te vergroten Volgende test mensheid:10 miljard voeden zonder de aarde te verpesten
Volgende test mensheid:10 miljard voeden zonder de aarde te verpesten Vlucht van fantasie? De luchtvaartindustrie probeert groen te worden
Vlucht van fantasie? De luchtvaartindustrie probeert groen te worden  Hoe kunnen adviseurs omgaan met sociale rechtvaardigheid te midden van de klimaatverandering?
Hoe kunnen adviseurs omgaan met sociale rechtvaardigheid te midden van de klimaatverandering?
Hoofdlijnen
- Houden schimmels geen mest uit planten?
- Welke plant bevat zowel mannelijke als vrouwelijke reproductieve structuren?
- Critici van positieve actie schilderen Aziatische Amerikanen af als de 'modelminderheid'. Waarom dat niet waar is
- Wat doet een luchtpijpcel?
- Wat gebeurt er met een dierlijke cel in een hypotone oplossing?
- Wat is de biologische naam van nostoc?
- Vier wetenschappelijke manieren om te zien of je kat van je houdt
- Welke cellen produceren GEEN celwanden?
- Hoe het bewustzijn bij dieren onderzocht zou kunnen worden
- Op klei gebaseerde antimicrobiële verpakking houdt voedsel vers

- Scherm van menselijke eiwitten onthult sommige met antimicrobiële kracht
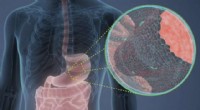
- Nieuw proces verandert papierproductieafval in waardevolle chemicaliën
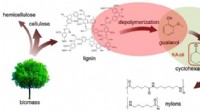
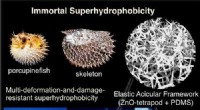
- Porcupinefish inspireert stevig superhydrofoob materiaal
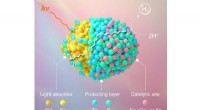
- Groeiende actieve sites op kwantumdots voor robuuste waterstoffotogeneratie
 Wiens vliegtuigexperiment hielp wetenschappers de principes van elektriciteit te begrijpen?
Wiens vliegtuigexperiment hielp wetenschappers de principes van elektriciteit te begrijpen?  Grenzen geen barrière voor thermo-elektriciteit
Grenzen geen barrière voor thermo-elektriciteit Een trein versnelt van 30 km per uur tot 45 in 15 seconden vindt het versnelling en afstand?
Een trein versnelt van 30 km per uur tot 45 in 15 seconden vindt het versnelling en afstand?  Watervervuiling kan economische groei met een derde verminderen:Wereldbank
Watervervuiling kan economische groei met een derde verminderen:Wereldbank MAXI J1348-630 is een zwart gat X-ray binaire, observaties suggereren:
MAXI J1348-630 is een zwart gat X-ray binaire, observaties suggereren: Rock Cycle-activiteiten voor studenten
Rock Cycle-activiteiten voor studenten Nanomaterialen bouwen voor computers van de volgende generatie
Nanomaterialen bouwen voor computers van de volgende generatie Koolstofbeprijzing werkt, blijkt uit groot metaonderzoek
Koolstofbeprijzing werkt, blijkt uit groot metaonderzoek
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

