
Wetenschap
Als u een geconcentreerde oplossing van zout verwarmt en deze neerslaat, is de voor deze exotherme of endotherm?
* Sout oplossen: Wanneer u zout in water oplost, is het proces endotherm. Het vereist energie om de ionische bindingen in het zoutkristal te breken en de ionen in de oplossing te scheiden.
* neerslag: Wanneer u een geconcentreerde zoutoplossing verwarmt, neemt de oplosbaarheid van het zout meestal toe. Naarmate de oplossing afkoelt, neemt de oplosbaarheid echter af. Dit betekent dat de zoutionen niet langer in oplossing kunnen worden gehouden en dat ze beginnen neer te slaan. Dit neerslagproces is ook endotherm omdat het energie vereist om de interacties tussen de zoutionen en de watermoleculen te breken.
Samenvattend:
* Verwarming: Aanvankelijk verhoogt het verwarmen van de oplossing de oplosbaarheid, wat een endotherme proces is.
* Koeling en neerslag: Naarmate de oplossing afkoelt, neemt de oplosbaarheid af, waardoor het zout wordt gedwongen om uit te slaan. Dit is ook een endotherme proces.
Daarom is het totale proces van het verwarmen van een geconcentreerde zoutoplossing en het veroorzaken van neerslag endotherm omdat het vereist dat energie -input plaatsvindt.
 Wat is het verzadigingspunt van citroenzuur en water?
Wat is het verzadigingspunt van citroenzuur en water?  Vergelijk en contrasteer hoe verschillen de chemische fysische eigenschappen?
Vergelijk en contrasteer hoe verschillen de chemische fysische eigenschappen?  Even kijken hoe ijsvorming voorruiten kan houden, hoogspanningsleidingen ijsvrij
Even kijken hoe ijsvorming voorruiten kan houden, hoogspanningsleidingen ijsvrij Het oxidatiegetal van chloor in de verbinding PbCl moet zijn?
Het oxidatiegetal van chloor in de verbinding PbCl moet zijn?  Is krijtverbindingsmengsel of een element?
Is krijtverbindingsmengsel of een element?
 Verschillen tussen noord- en zuidhellingen
Verschillen tussen noord- en zuidhellingen  Elk object dat om een ander draait, is een?
Elk object dat om een ander draait, is een?  The Scream:Wat waren die kleurrijke, golvende wolken in het beroemde schilderij van Edvard Munch?
The Scream:Wat waren die kleurrijke, golvende wolken in het beroemde schilderij van Edvard Munch? Het eerste voorbeeld van recycling op aarde:zijn eigen korst
Het eerste voorbeeld van recycling op aarde:zijn eigen korst Veengebieden zullen meer koolstof opslaan naarmate de planeet opwarmt
Veengebieden zullen meer koolstof opslaan naarmate de planeet opwarmt
Hoofdlijnen
- Hoe wordt het genoemd als wetenschapper een gok doet?
- Wat is een andere vorm van transport die eiwitten gebruikt om andere ionen en kleine moleculen over het plasmamembraan te verplaatsen?
- Kunnen ziektedetecterende honden de dikhoornschapen in South Dakota helpen redden?
- Hoe een jetlag werkt
- Welke fase van een cellencyclus lijnen de gerepliceerde chromosomen op de evenaarcel?
- Er komen aanwijzingen naar voren:hoe ongevaarlijke bacteriën zich ontwikkelen tot dodelijke vleesetende varianten
- Hoe een tRNA-reeks te krijgen van een DNA-reeks
- Welk levenloos object is in staat om ziekten over te dragen?
- Hoe wordt het ene geslacht groter dan het andere?
- Nieuwe kleurstoffen detecteren ziekte door hartslagsignalen

- Collectieve ontvlechting van verstrengelde polymeren

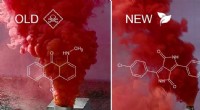
- Een groener alternatief voor roodgekleurde rook
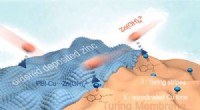
- Turing-membraan om de prestaties van op zink gebaseerde batterijen te verbeteren
- Kijken naar atomen die bewegen in hybride perovskietkristallen onthult aanwijzingen voor het verbeteren van zonnecellen

 Hoe kan een veranderend klimaat de menselijke vruchtbaarheid beïnvloeden?
Hoe kan een veranderend klimaat de menselijke vruchtbaarheid beïnvloeden?  EarthCARE-satelliet om te onderzoeken hoe wolken het klimaat beïnvloeden
EarthCARE-satelliet om te onderzoeken hoe wolken het klimaat beïnvloeden  Hoe AI onze relatie met religie zou kunnen veranderen
Hoe AI onze relatie met religie zou kunnen veranderen  Noord-Amerikaanse waterwegen worden zouter en alkalischer
Noord-Amerikaanse waterwegen worden zouter en alkalischer Zuurstofverlies in de kust van de Oostzee is ongekend ernstig
Zuurstofverlies in de kust van de Oostzee is ongekend ernstig Wat is de meest voorkomende materietoestand voor water?
Wat is de meest voorkomende materietoestand voor water?  Astronomen ontdekken dat minstens één op de tien sterren tekenen vertoont van planetaire opname
Astronomen ontdekken dat minstens één op de tien sterren tekenen vertoont van planetaire opname  Enkelstrengs DNA als supramoleculaire sjabloon voor sterk georganiseerde palladium-nanodraden
Enkelstrengs DNA als supramoleculaire sjabloon voor sterk georganiseerde palladium-nanodraden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

