
Wetenschap
Helpermoleculen in de chemische reactie?
Hier is een uitsplitsing:
katalysatoren
* Definitie: Katalysatoren zijn stoffen die de snelheid van een chemische reactie verhogen zonder tijdens het proces te worden geconsumeerd.
* mechanisme: Katalysatoren werken door een alternatieve reactieroute te bieden met een lagere activeringsenergie. Dit betekent dat er minder energie voor nodig is om de reactanten te bereiken om de overgangstoestand te bereiken en producten te vormen.
* typen: Er zijn verschillende soorten katalysatoren, waaronder:
* enzymen: Biologische katalysatoren die typisch eiwitten zijn. Ze zijn zeer specifiek voor hun substraten (reactanten) en werken vaak in complexe systemen in cellen.
* anorganische katalysatoren: Deze omvatten metalen, metaaloxiden en andere anorganische verbindingen. Ze worden vaak gebruikt in industriële processen.
* heterogene katalysatoren: Deze katalysatoren bevinden zich in een andere fase (vast, vloeistof of gas) dan de reactanten.
* Homogene katalysatoren: Deze katalysatoren bevinden zich in dezelfde fase als de reactanten.
Andere helpermoleculen
Naast katalysatoren zijn er andere moleculen die ondersteunende rollen kunnen spelen in chemische reacties:
* Co -enzymen: Dit zijn niet-eiwit organische moleculen die enzymen helpen bij hun katalytische activiteit. Ze dragen vaak elektronen of functionele groepen.
* Cofactors: Dit zijn anorganische moleculen die enzymen helpen bij hun katalytische activiteit. Het kunnen metaalionen of andere kleine moleculen zijn.
* Mediators: Deze moleculen kunnen helpen bij het overbrengen van reactanten of producten van het ene deel van de reactie op het andere.
voorbeelden
* enzymen: Het enzymlactase breekt lactose (melksuiker) af in glucose en galactose.
* anorganische katalysatoren: Het Haber-Bosch-proces voor het produceren van ammoniak maakt gebruik van een ijzeren katalysator.
* Co -enzymen: NAD+ (nicotinamide adenine dinucleotide) is een co -enzym dat een sleutelrol speelt in veel metabole reacties.
* Cofactors: Zinkionen zijn een cofactor voor het enzym -koolhydrase.
belangrijke opmerkingen:
* Katalysatoren worden niet geconsumeerd in de reactie, maar kunnen worden hergebruikt.
* Katalysatoren veranderen het evenwicht van een reactie niet; Ze versnellen alleen de snelheid waarmee het evenwicht bereikt.
* De aanwezigheid van een katalysator kan de snelheid van een reactie aanzienlijk beïnvloeden, zelfs onder milde omstandigheden.
Ik hoop dat deze uitleg helpt! Als je nog meer vragen hebt, stel je gerust.
 NASA vindt tropische depressie 23Ws sterkste stormen in twee landen
NASA vindt tropische depressie 23Ws sterkste stormen in twee landen De luchtverontreinigingsniveaus van Pittsburgh daalden tijdens de thuisbestelling, maar de algehele impact blijft klein
De luchtverontreinigingsniveaus van Pittsburgh daalden tijdens de thuisbestelling, maar de algehele impact blijft klein Californiërs bashen Trump voor poging om klimaatveranderingsplan te beëindigen
Californiërs bashen Trump voor poging om klimaatveranderingsplan te beëindigen Hoe worden soorten gesorteerd in de verschillende koninkrijken?
Hoe worden soorten gesorteerd in de verschillende koninkrijken?  Na de bosbranden hielpen we bij het uitkiezen van de dieren en planten die het meest nodig waren. Hier is hoe het gebeurde
Na de bosbranden hielpen we bij het uitkiezen van de dieren en planten die het meest nodig waren. Hier is hoe het gebeurde
Hoofdlijnen
- Hoe u een mRNA-reeks kunt berekenen
- Welke dieren kunnen het coronavirus oplopen?
- Wat is de eenheid van natuurlijke selectie?
- Als dieren sterven, hoe beïnvloedt dit dan uw voedselketen?
- Wat zijn de vier stappen van theorie -evolutie?
- Droogteresistente plantengenen kunnen de evolutie van waterbesparende gewassen versnellen
- Onderzoek onderzoekt hoe beslissingen over embryonale ontwikkeling tegelijkertijd door meerdere routes worden gecontroleerd
- Hoe sperma het genoom van vader uitpakt, zodat het kan samensmelten met dat van moeder
- Beschrijf de waarschijnlijke effecten op een ecosysteem als alle ontleders zouden sterven?
- Onderzoekers brengen eiwitbeweging in kaart
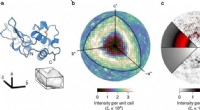
- Power-to-gas-installatie met hoog rendement

- Wetenschappers kijken naar vetmetabolisme in levende vissen, observeer real-time lipidenbiochemie
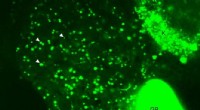
- Communicatie verstoren bij infectieuze bacteriën
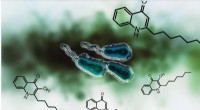
- De zuurtest doorstaan:nieuw systeem met lage pH recyclet meer koolstof in waardevolle producten

 Wat zijn enkele carnivoren in de Great Plains?
Wat zijn enkele carnivoren in de Great Plains?  Lancering nadert voor NASA's volgende Marsrover, Doorzettingsvermogen
Lancering nadert voor NASA's volgende Marsrover, Doorzettingsvermogen Waarom bevindt Hawaii zich niet op een plaatgrens?
Waarom bevindt Hawaii zich niet op een plaatgrens?  Welke zee is 41 graden North Latitude en 28 East Loogte?
Welke zee is 41 graden North Latitude en 28 East Loogte?  Hoeveel pond in 480 ounces?
Hoeveel pond in 480 ounces?  Wat gebeurt er met de temperatuur en de druk als de diepte onder het aardoppervlak toeneemt?
Wat gebeurt er met de temperatuur en de druk als de diepte onder het aardoppervlak toeneemt?  Wat is euchaebacteriën?
Wat is euchaebacteriën?  Watchdog:FBI had harder kunnen proberen om iPhone te hacken
Watchdog:FBI had harder kunnen proberen om iPhone te hacken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

