
Wetenschap
Wat is de conditie koud geeft pertaal in welke wetten stadium die bij de gegeven temperatuur oplosbaarheid van gas recht proportioneel perciaal drukgas rechtstreeks?
Hier is een uitsplitsing:
* Oplosbaarheid: De hoeveelheid gas die kan oplossen in een vloeistof bij een gegeven temperatuur en druk.
* Gedeeltelijke druk: De druk uitgeoefend door een specifiek gas in een mengsel van gassen.
* recht evenredig: Dit betekent dat naarmate de gedeeltelijke druk van het gas toeneemt, de oplosbaarheid van het gas in de vloeistof ook evenredig toeneemt.
in eenvoudiger termen:
Denk aan een blikje frisdrank. Wanneer u deze opent, wordt de druk binnen vrijgegeven, waardoor de opgeloste koolstofdioxide (CO2) ontsnapt als bubbels. Dit gebeurt omdat de gedeeltelijke druk van CO2 boven de vloeistof afneemt, wat op zijn beurt de oplosbaarheid in de frisdrank vermindert.
Sleutelpunten:
* De wet van Henry is alleen van toepassing op gassen opgelost in vloeistoffen.
* De temperatuur wordt gehouden constant in deze wet.
* De evenredigheidsconstante (constante wet van Henry) hangt af van het specifieke gas en de vloeistof.
Voorbeeld:
Als u de gedeeltelijke zuurstofdruk boven een waterlichaam verhoogt, zal meer zuurstof in het water oplossen. Dit is de reden waarom vissen kunnen overleven in dieper water waar de druk hoger is.
Laat het me weten als je nog andere vragen hebt!
 Efficiënte elektrokatalytische reductie van nitraat tot stikstof:veelbelovende manier om stikstof uit water te verwijderen
Efficiënte elektrokatalytische reductie van nitraat tot stikstof:veelbelovende manier om stikstof uit water te verwijderen Video:Wat zou Trump kunnen betekenen voor de chemie?
Video:Wat zou Trump kunnen betekenen voor de chemie?  Is ijzer is elementverbinding of mengsel?
Is ijzer is elementverbinding of mengsel?  Is chloor moleculair ionisch of metallisch?
Is chloor moleculair ionisch of metallisch?  Ontworpen elektrodemateriaal brengt de ontwikkeling van de batterij dichter bij snel opladen
Ontworpen elektrodemateriaal brengt de ontwikkeling van de batterij dichter bij snel opladen
 NASA kijkt toe hoe tropische storm Ileana verzwakt door twee factoren
NASA kijkt toe hoe tropische storm Ileana verzwakt door twee factoren Klimaatverandering kan meer sediment en vervuiling opleveren voor de San Francisco Bay-Delta
Klimaatverandering kan meer sediment en vervuiling opleveren voor de San Francisco Bay-Delta Afnemende sneeuwlaag boven het westen van de VS op een fijnere schaal in kaart gebracht
Afnemende sneeuwlaag boven het westen van de VS op een fijnere schaal in kaart gebracht Planten die giftig zijn voor doosschildpadden
Planten die giftig zijn voor doosschildpadden  Rivier-grondwater hotspot voor arseen
Rivier-grondwater hotspot voor arseen
Hoofdlijnen
- Eerste onderzoek dat aantoont dat vogels en niet alleen zoogdieren geeuwen kopiëren
- Is diepgevroren kabeljauw net zo lekker als vers?
- Wat is de betekenis van fysisch?
- Voorbeeld van oorzaak en gevolghypothese?
- Wat zijn de locomotaire organellen in Paramecium en Euglena?
- Waarom hebben de meeste mensen 23 paar chromosomen?
- Noem de organisatieniveaus in de ecologie, te beginnen met de biosfeer?
- Het nepnieuwsprobleem van Facebook:wat is de verantwoordelijkheid ervan?
- Wat is de vorm van locomotie univalen?
- Een snellere en betrouwbaardere methode om olijfolie te categoriseren is gevalideerd

- Superieure bio-inkt voor 3D-printen pionier
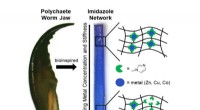
- Wetenschappers bootsen de dodelijke kaak van een worm na om veerkrachtige materialen te ontwerpen en te vormen
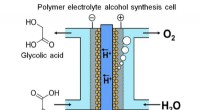
- Onderzoek naar elektrolyse voor energieopslag
- Stromend zout water over dit superhydrofobe oppervlak kan elektriciteit opwekken
 Hoe klimaatverandering de Colombiaanse koffieproductie beïnvloedt
Hoe klimaatverandering de Colombiaanse koffieproductie beïnvloedt  Wat zijn twee manieren om erosie te voorkomen of te vertragen?
Wat zijn twee manieren om erosie te voorkomen of te vertragen?  Sensoren op plantenbladeren waarschuwen voor watertekort
Sensoren op plantenbladeren waarschuwen voor watertekort Wat is het broeikasgas dat de opwarming van de aarde versnelt?
Wat is het broeikasgas dat de opwarming van de aarde versnelt?  Hoe snel kunnen vingers bewegen?
Hoe snel kunnen vingers bewegen?  VS waarschuwt voor WTO-actie wegens discriminerende nieuwe digitale belastingen
VS waarschuwt voor WTO-actie wegens discriminerende nieuwe digitale belastingen Enorme Outback-rotskunstsite onthult oud verhaal
Enorme Outback-rotskunstsite onthult oud verhaal  Exoplanet-ontdekkingstool begint zijn missie
Exoplanet-ontdekkingstool begint zijn missie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

