
Wetenschap
Is de binding tussen magnesium en zuurstof een ionisch of herstellend?
* Elektronegativiteitsverschil: Magnesium (mg) heeft een elektronegativiteit van 1,31, terwijl zuurstof (O) een elektronegativiteit van 3,44 heeft. Het verschil in elektronegativiteit is significant (2.13), wat duidt op een sterke neiging voor zuurstof om elektronen aan te trekken.
* elektronenoverdracht: Magnesium verliest gemakkelijk zijn twee valentie -elektronen om een stabiel octet te bereiken. Zuurstof daarentegen krijgt die twee elektronen om zijn octet te voltooien. Deze elektronenoverdracht vormt positief geladen magnesiumionen (mg²⁺) en negatief geladen oxide -ionen (o²⁻).
* Elektrostatische aantrekkingskracht: De tegenovergestelde ladingen van de ionen trekken elkaar aan en vormen een elektrostatische binding die bekend staat als een ionische binding.
Daarom is de binding tussen magnesium en zuurstof in magnesiumoxide (MGO) voornamelijk ionisch.
 Wat is een natuurlijke selectie van een olifanten?
Wat is een natuurlijke selectie van een olifanten?  Het vertellen van verhalen in de metaverse kan milieuactie stimuleren
Het vertellen van verhalen in de metaverse kan milieuactie stimuleren  Een nieuwe kijk op de grote lenteschoonmaak-waanzin:hoe het bewaren van oude dingen op zijn eigen manier 'vreugde kan opwekken'
Een nieuwe kijk op de grote lenteschoonmaak-waanzin:hoe het bewaren van oude dingen op zijn eigen manier 'vreugde kan opwekken'  Door oorlog verscheurd Zuid-Soedan loopt groot risico op klimaatverandering
Door oorlog verscheurd Zuid-Soedan loopt groot risico op klimaatverandering Welke organismen vertonen cefalisatie?
Welke organismen vertonen cefalisatie?
Hoofdlijnen
- Wat is de betekenis van de biologie van reproductieve klonen?
- Wat is de functie van pacesettercellen?
- Waarom hebben lever- en spiercellen meer mitochondriën dan andere soorten cellen?
- Onderzoek biedt belangrijk inzicht in hoe cellen fuseren
- Wat maakt de aarde precies goed voor leven?
- Anatomische structuren: homoloog, analoog & vestigiaal
- Wetenschappers ontwikkelen nieuwe technieken om te volgen hoe cellen functioneren
- Welke immuniteit resulteert wanneer miljoenen geheugen B -cellen in het lichaam blijven?
- Wat is een voorbeeld van een kanaaleiwit?
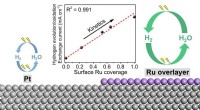
- Nieuwe mechanismen voor verbetering van de activiteit van bimetaalkatalysatoren voor waterstofopwekking en brandstofcellen
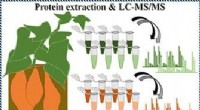
- Het proteoom van de zoete aardappel opgraven
- Snelste zeer nauwkeurige 3D-printer

- Nieuwe theorie ontsluit het geheim achter eiwit-membraan-interacties

- Voorkomen van infectie, genezing vergemakkelijken:nieuwe biomaterialen van spinnenzijde

 Onderzoek toont aan dat geothermie een ideale technologie voor energieopslag kan zijn
Onderzoek toont aan dat geothermie een ideale technologie voor energieopslag kan zijn Gaan de dermale strengen weefsels voedselwater en mineralen?
Gaan de dermale strengen weefsels voedselwater en mineralen?  Hoe zeepaardjes ademen
Hoe zeepaardjes ademen  Voorbeelden van de eerste wet van bewegingswet?
Voorbeelden van de eerste wet van bewegingswet?  Hoe je van een vulkaan een krachtcentrale maakt – met een beetje hulp van satellieten
Hoe je van een vulkaan een krachtcentrale maakt – met een beetje hulp van satellieten Waarom ijs meestal bewolkt bevriest,
Waarom ijs meestal bewolkt bevriest,  Wat is de kracht die een leerling uitoefent als hij een massa van 40 kg heeft en versnelt met een snelheid van 2 meter per seconde?
Wat is de kracht die een leerling uitoefent als hij een massa van 40 kg heeft en versnelt met een snelheid van 2 meter per seconde?  Kindergarten Games voor Identifying Numbers 1-20
Kindergarten Games voor Identifying Numbers 1-20
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

