
Wetenschap
Verbinding gemaakt van 63,50 zilver, 8,25 stikstof en 28,25 zuurstof met een totale molmassa van 169,91 g?
1. Bereken de molaire massa van elk element:
- Zilver (Ag):Molaire massa =107,87 g/mol
- Stikstof (N):Molaire massa =14,01 g/mol
- Zuurstof (O):Molaire massa =16,00 g/mol
2. Bereken het aantal mol van elk element:
- Mol Ag =63,50 g / 107,87 g/mol =0,588 mol
- Mol N =8,25 g / 14,01 g/mol =0,589 mol
- Mol O =28,25 g / 16,00 g/mol =1,766 mol
3. Bepaal de relatieve verhoudingen van elk element:
- Ag:0,588 mol / 1,766 mol =0,333
- N:0,589 mol / 1,766 mol =0,334
- O:1,766 mol / 1,766 mol =1
4. Vereenvoudig de relatieve verhoudingen om hele getallen te verkrijgen:
- Ag:0,333 ≈ 1
- N:0,334 ≈ 1
- O:1
5. De empirische formule van de verbinding is AgNO.
6. Bereken de empirische formulemassa:
Empirische formule massa (AgNO) =(1 x 107,87 g/mol) + (1 x 14,01 g/mol) + (1 x 16,00 g/mol) =169,88 g/mol
De berekende massa van de empirische formule ligt zeer dicht bij de gegeven totale molaire massa van 169,91 g, wat erop wijst dat de empirische formule correct is.
 NASA krijgt infraroodbeeld van de subtropische storm van Atlantische Halloween
NASA krijgt infraroodbeeld van de subtropische storm van Atlantische Halloween Onderzoeker ontdekt nieuwe route voor warmtetransport in oceaan
Onderzoeker ontdekt nieuwe route voor warmtetransport in oceaan Invasieve vuurstarter:hoe niet-inheemse grassen Hawaï in een tondeldoos veranderden
Invasieve vuurstarter:hoe niet-inheemse grassen Hawaï in een tondeldoos veranderden  Klimaat in een zoetwaterbiomeer
Klimaat in een zoetwaterbiomeer  Meer dan 100 brandweerwetenschappers dringen er bij het westen van de VS op aan:sla het vuurwerk over op deze recorddroge 4 juli
Meer dan 100 brandweerwetenschappers dringen er bij het westen van de VS op aan:sla het vuurwerk over op deze recorddroge 4 juli
Hoofdlijnen
- Onderzoekers ontdekken details over hoe bacteriën beschermende barrières bouwen, wat nieuwe antibiotica kan opleveren
- Hoe maak je een werkend hart Model
- Wat de mechanische krachten achter eiwitvouwing ons kunnen vertellen over uitgezaaide kanker
- Jonge, koelbloedige dieren lijden het meest door de opwarming van de aarde, blijkt uit onderzoek
- Nieuwe aanwijzingen over hoe planten gezonde genomen behouden en mitochondriale ziekten vermijden
- Hoe de ijstijden de evolutie van de vreemde en stugge inheemse planten in Nieuw-Zeeland hebben gestimuleerd
- Een groot herhalend molecuul kan het leven bepalen
- Reuzenberenklauwsap kan je zonnebrand geven
- Is een hoorn des overvloeds homogeen of heterogeen?
- Chemici leren neurale netwerken om eigenschappen van verbindingen te voorspellen
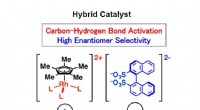
- Hybride katalysator met hoge enantiomeerselectiviteit
- Enzymstructuren verlichten het mechanisme achter de bioremediatie van bacteriën

- Het plastictekort oplossen met een nieuwe chemische katalysator
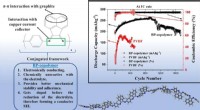
- Nieuw copolymeerbindmiddel om de levensduur van lithium-ionbatterijen te verlengen
 Hoeveel mol kooldioxide wordt gevormd uit 14 methaan?
Hoeveel mol kooldioxide wordt gevormd uit 14 methaan?  Zagat op menu voor restaurantbeoordelingssite Infatuation (update)
Zagat op menu voor restaurantbeoordelingssite Infatuation (update) Hoe de hoekpunten van een ellips te vinden
Hoe de hoekpunten van een ellips te vinden Wetenschappers zetten primaten tegenover zoogdieren met kleinere hersenen om erachter te komen wie de slimste verzamelaar is
Wetenschappers zetten primaten tegenover zoogdieren met kleinere hersenen om erachter te komen wie de slimste verzamelaar is  Welke invloed heeft waterkrachtenergie op het milieu?
Welke invloed heeft waterkrachtenergie op het milieu?  Hoe werkt een veerweger?
Hoe werkt een veerweger?  Hoe NASA's Mars-helikopter het oppervlak van de rode planeten zal bereiken
Hoe NASA's Mars-helikopter het oppervlak van de rode planeten zal bereiken GTEx Consortium geeft nieuwe inzichten vrij in de manier waarop DNA-verschillen de genexpressie bepalen
GTEx Consortium geeft nieuwe inzichten vrij in de manier waarop DNA-verschillen de genexpressie bepalen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

