
Wetenschap
Hoeveel mol calciumoxide wordt geproduceerd als 36,5 gram volledig reageert met zuurstofgas?
$$2Ca(s) + O_2(g) → 2CaO(s)$$
Uit de vergelijking kunnen we zien dat 2 mol calcium reageren met 1 mol zuurstof om 2 mol calciumoxide te produceren.
Eerst moeten we de gegeven massa calcium (36,5 gram) omzetten in mol. De molaire massa van calcium is 40,08 g/mol.
$$36,5 \text{ g Ca} \times \frac{1 \text{ mol Ca}}{40,08 \text{ g Ca}} =0,910 \text{ mol Ca}$$
Vervolgens moeten we de beperkende reactant bepalen. Om dit te doen, vergelijken we het aantal beschikbare mol calcium en zuurstof.
Ervan uitgaande dat we voldoende zuurstofgas hebben, kunnen we het maximale aantal mol calciumoxide berekenen dat kan worden geproduceerd met behulp van het aantal mol calcium:
$$0,910 \text{ mol Ca} \times \frac{2 \text{ mol CaO}}{2 \text{ mol Ca}} =0,910 \text{ mol CaO}$$
Daarom zal er 0,910 mol calciumoxide worden geproduceerd wanneer 36,5 gram calcium volledig reageert met zuurstofgas.
 Hoeveel moleculen ethaan zijn aanwezig in 0,334 g C2 H6?
Hoeveel moleculen ethaan zijn aanwezig in 0,334 g C2 H6?  Wat is een calorimeter en wat zijn de beperkingen?
Wat is een calorimeter en wat zijn de beperkingen?  Welk paar elementen heeft de meest vergelijkbare chemische eigenschappen?
Welk paar elementen heeft de meest vergelijkbare chemische eigenschappen?  Hoe de dikke darm prioriteit geeft aan gasontgifting boven energieverbruik?
Hoe de dikke darm prioriteit geeft aan gasontgifting boven energieverbruik? Bepalen hoe en waarom cellen beslissingen nemen
Bepalen hoe en waarom cellen beslissingen nemen
 Waarom vrouwelijke waterbuffels hoorns hebben, maar impala's niet?
Waarom vrouwelijke waterbuffels hoorns hebben, maar impala's niet?  Greta Thunberg:het jeugdige klimaatgeweten ter wereld
Greta Thunberg:het jeugdige klimaatgeweten ter wereld Nieuwe studie vindt dat het overstromingsrisico voor Amerikanen sterk wordt onderschat
Nieuwe studie vindt dat het overstromingsrisico voor Amerikanen sterk wordt onderschat Het verhogen van de pH van de bodem vermindert de uitstoot van stikstofoxide afkomstig van kunstmest
Het verhogen van de pH van de bodem vermindert de uitstoot van stikstofoxide afkomstig van kunstmest Welke invloed zal de klimaatverandering op uw levensonderhoud hebben?
Welke invloed zal de klimaatverandering op uw levensonderhoud hebben?
Hoofdlijnen
- Een universele voedsel- en alarmsignaal gevonden in zoogdierbloed
- Het is moeilijk om fossiele huid te vinden, maar een zeldzame ontdekking onthult aanwijzingen over de evolutie van water naar land
- Hoe ziekteverwekkers mitochondriale afweermechanismen kunnen uitschakelen
- Wat is de biologische levenscyclus van vleermuizen?
- Wilde druivengist kan effectiever zijn dan pesticiden bij het voorkomen van druivenschimmels
- Bevordering van de veerkracht van fruitgewassen:onthulling van de moleculaire dynamiek van abscissie in houtachtige fruitgewassen
- Wat concludeerde Thomas Hunt Morgan over de chromosomen van de fruitvlieg?
- Wetenschappers onderzoeken het vermogen van prikken om zich aan te passen en te overleven
- Hoe hybride plantenrassen de uitdagingen van voedselzekerheid en klimaatverandering kunnen aanpakken
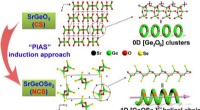
- Nieuwe gedeeltelijke isovalente inductiestrategie voor anionsubstitutie om infrarood niet-lineaire optische materialen te ontwerpen
- CO2 omzetten om duurzame energie op te slaan

- Oppervlakken die als gekkovoeten vastgrijpen, kunnen gemakkelijk in massa worden geproduceerd

- Ammoniumnitraat en jodium:een terugblik op de explosieve geschiedenis van twee essentiële stoffen

- Bewaar ambachtelijk bier op een koele plaats en consumeer het zo vers mogelijk

 Wervelende spiralen op de noordpool van Mars
Wervelende spiralen op de noordpool van Mars Op zoek naar leven op Enceladus:welke vragen moeten we stellen?
Op zoek naar leven op Enceladus:welke vragen moeten we stellen?  Eerdere theorieën over hoe elektronen bewegen binnen eiwit-nanokristallen zijn mogelijk niet in alle gevallen van toepassing
Eerdere theorieën over hoe elektronen bewegen binnen eiwit-nanokristallen zijn mogelijk niet in alle gevallen van toepassing  NASA Artemis1 om ASU CubeSat de ruimte in te dragen
NASA Artemis1 om ASU CubeSat de ruimte in te dragen Het high-stakes spel van geo-engineering heeft tot doel dreigende klimaatrampen te verminderen
Het high-stakes spel van geo-engineering heeft tot doel dreigende klimaatrampen te verminderen De manier waarop we water in ons lichaam transporteren, inspireert tot een nieuwe filtratiemethode
De manier waarop we water in ons lichaam transporteren, inspireert tot een nieuwe filtratiemethode  Computermodellen van tornado's tonen een mogelijk schuilgebied achter heuvels
Computermodellen van tornado's tonen een mogelijk schuilgebied achter heuvels  Amazon lanceert winkel voor kleine bedrijven
Amazon lanceert winkel voor kleine bedrijven
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

