
Wetenschap
Een dynamisch evenwicht wordt bereikt wanneer waterstofcyanidezuur oplost in water. Welke soort heeft de hoogste concentratie in deze oplossing?
Wanneer waterstofcyanide (HCN) wordt opgelost in water, ondergaat het een chemische reactie met watermoleculen om blauwzuur (HCN(aq)) en hydroxide-ionen (OH-) te vormen volgens de volgende evenwichtsvergelijking:
HCN(aq) + H2O(l) <=> H3O+(aq) + CN-(aq)
In dit evenwicht is de soort met de hoogste concentratie water (H2O). Water is het oplosmiddel in dit systeem en is in veel grotere concentraties aanwezig dan bij de andere soorten. De waterconcentratie blijft tijdens de reactie vrijwel constant.
De concentraties van HCN(aq), H3O+(aq) en CN-(aq) zijn relatief laag vergeleken met de concentratie van water. De evenwichtsconstante voor deze reactie is erg klein, wat erop wijst dat de reactie beperkt verloopt. Daarom blijft het merendeel van de HCN-moleculen ongereageerd en opgelost in het water.
 Eco-lijm kan schadelijke lijmen in houtconstructies vervangen
Eco-lijm kan schadelijke lijmen in houtconstructies vervangen Wat is de chemische vergelijking voor de ontleeding van ammoniumnitraat in stikstof en water?
Wat is de chemische vergelijking voor de ontleeding van ammoniumnitraat in stikstof en water?  Welk type binding zal plaatsvinden tussen magnesiumatoom en een zuurstofatoom?
Welk type binding zal plaatsvinden tussen magnesiumatoom en een zuurstofatoom?  Welke mineralen zitten er in papieren handdoeken?
Welke mineralen zitten er in papieren handdoeken?  Veel oude boeken bevatten giftige chemicaliën. Zo kun je ze herkennen
Veel oude boeken bevatten giftige chemicaliën. Zo kun je ze herkennen
 De onzekere toekomst van de oceanen
De onzekere toekomst van de oceanen Onderzoek toont aan welk soort zout we in de winter op de wegen gebruiken, een verschil kan maken voor planten
Onderzoek toont aan welk soort zout we in de winter op de wegen gebruiken, een verschil kan maken voor planten  Kliffen storten in bij vulkaan Hawaï, het stoppen van de brandslangstroom
Kliffen storten in bij vulkaan Hawaï, het stoppen van de brandslangstroom Hoe een Raven Feather
Hoe een Raven Feather Nauwkeurige zelfbeoordeling:hoe de sociale omgeving dit vermogen bij kinderen beïnvloedt
Nauwkeurige zelfbeoordeling:hoe de sociale omgeving dit vermogen bij kinderen beïnvloedt
Hoofdlijnen
- Hebben alle levende wezens cellen?
- 245 miljoen jaar oude fossielen bieden nieuwe inzichten in de evolutie en voedingsstrategieën van waterinsecten
- Wat zegt Darwins evolutietheorie?
- GoT-ChA:Nieuw hulpmiddel onthult hoe genmutaties cellen beïnvloeden
- Bijenzoemen kunnen helpen bepalen hoe ze hun afnemende populatie kunnen redden
- Vreemde zijde:waarom abseilende spinnen niet uit de hand lopen
- Ecologische soortvorming door seksuele selectie op goede genen:is adaptief?
- Mengen de Atlantische en de Stille Oceaan zich?
- Welke omstandigheden kunnen de groei van bacteriën hebben bevorderd?
- Malariapathogeen onder de röntgenmicroscoop
- Waardoor ontstaat die piek? Een al lang bestaande vraag over covalente vloeistoffen beantwoorden
- Een prebiotische route naar DNA
- Heilige graal voor batterijen:Solid-state magnesiumbatterij een grote stap dichterbij
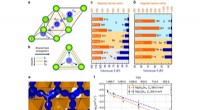
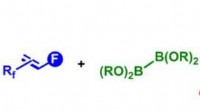
- Chemici ontsluiten het potentieel van fluoralkenen
 Hoe geconnecteerde ruitenwissers van voertuigen overstromingen kunnen voorkomen
Hoe geconnecteerde ruitenwissers van voertuigen overstromingen kunnen voorkomen Zal het geplande zonneveld van China de kosten van alternatieve energie verlagen?
Zal het geplande zonneveld van China de kosten van alternatieve energie verlagen?  Wat zijn enkele voorbeelden van de problemen waarmee astronomen te maken krijgen bij hun ruimteverkenning?
Wat zijn enkele voorbeelden van de problemen waarmee astronomen te maken krijgen bij hun ruimteverkenning?  Natuurlijke seismometers bevestigd op zeebodem
Natuurlijke seismometers bevestigd op zeebodem Magnetisatie regelen door akoestische oppervlaktegolven
Magnetisatie regelen door akoestische oppervlaktegolven Onderzoek toont aan dat temperatuur het gedrag van 2D-materialen drastisch kan beïnvloeden
Onderzoek toont aan dat temperatuur het gedrag van 2D-materialen drastisch kan beïnvloeden Hoe zijn atomen verbonden met een element?
Hoe zijn atomen verbonden met een element?  Waarin verschilt een verbinding van een element?
Waarin verschilt een verbinding van een element?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

