
Wetenschap
Hoe breng je H2O2 - H2O in balans?
2 H2O2(l) → 2 H2O(l) + O2(g)
Uitleg :
In de onevenwichtige vergelijking hebben we:
Reactanten: 2 H2O2(l)
Product: 2 H2O(l)
Om de vergelijking in evenwicht te brengen, moeten we coëfficiënten toevoegen aan de reactanten en producten om ervoor te zorgen dat het aantal atomen van elk element aan beide kanten van de vergelijking hetzelfde is.
Stap 1:Breng waterstofatomen (H) in evenwicht:
Aan de kant van de reactanten hebben we 4 H-atomen uit 2 H2O2-moleculen. Aan de productzijde hebben we 4 H-atomen uit 2 H2O-moleculen. De vergelijking is al in evenwicht met betrekking tot H-atomen.
Stap 2:Breng de zuurstofatomen (O) in evenwicht:
Aan de kant van de reactanten hebben we 4 O-atomen uit 2 H2O2-moleculen. Aan de productzijde hebben we 2 O-atomen uit 2 H2O-moleculen en 2 O-atomen uit het O2-molecuul. We kunnen O-atomen in evenwicht brengen door een coëfficiënt van 2 vóór H2O2 toe te voegen.
Uitgebalanceerde vergelijking :
2 H2O2(l) → 2 H2O(l) + O2(g)
Nu is de vergelijking in evenwicht, met 4 H-atomen en 6 O-atomen aan beide kanten.
 MIT-analyse laat zien hoe cap-and-trade-plannen de uitstoot van broeikasgassen kunnen terugdringen
MIT-analyse laat zien hoe cap-and-trade-plannen de uitstoot van broeikasgassen kunnen terugdringen  Wetenschappers vinden nieuwe manieren om chemicaliën voor bioraffinage te gebruiken
Wetenschappers vinden nieuwe manieren om chemicaliën voor bioraffinage te gebruiken Hoe worden buigrietjes gemaakt?
Hoe worden buigrietjes gemaakt?  Natuurkundestudent ontwikkelt machine learning-model voor energie- en milieutoepassingen
Natuurkundestudent ontwikkelt machine learning-model voor energie- en milieutoepassingen Het beheersen van de nanoschaalstructuur van membranen is essentieel voor schoon water, onderzoekers vinden
Het beheersen van de nanoschaalstructuur van membranen is essentieel voor schoon water, onderzoekers vinden
 Waarom heeft iedereen het over natuurlijke sequentielandbouw?
Waarom heeft iedereen het over natuurlijke sequentielandbouw? Arctische planten bieden mogelijk geen voorspeld koolstofvastleggingspotentieel
Arctische planten bieden mogelijk geen voorspeld koolstofvastleggingspotentieel Koolstofmarkt kan de enorme rekening voor brandherstel in Australië compenseren
Koolstofmarkt kan de enorme rekening voor brandherstel in Australië compenseren IJskap smelt:schattingen nog onzeker, experts waarschuwen
IJskap smelt:schattingen nog onzeker, experts waarschuwen Onderzoekers onderzoeken waarom de dode zone Lake Erie teruggaf
Onderzoekers onderzoeken waarom de dode zone Lake Erie teruggaf
Hoofdlijnen
- 'Als een tunnel voor cholesterol':Wetenschappers laten zien hoe 'slechte' cholesterol in de cellen terechtkomt
- Hoe begint vervanging in DNA?
- Oesterschelpen worden voor topprijzen verkocht terwijl biologen zich inspannen om schelpdierbanken te beschermen
- Stamcellen tonen de kracht om ziekten en medicijntoxiciteit te voorspellen
- Waarom een extra helix een derde wiel wordt in de celbiologie
- Onderbroken herprogrammering zet volwassen cellen om in hoge opbrengsten van voorloperachtige cellen
- Onderzoekstopics in Biotechnology
- Hoeveel ziekten veroorzaakt door platwormen?
- Hoe fittere vissen meer mensen kunnen voeden te midden van voedselonzekerheid
- Destabilisatieprocessen in schuim

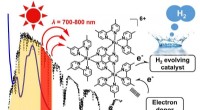
- NIR-gestuurde H2-evolutie uit water:uitbreidend golflengtebereik voor omzetting van zonne-energie
- Meervoudige aanval van virussen op bacteriën wijst op nieuwe manieren om infecties te bestrijden
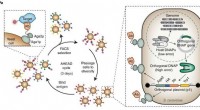
- Nieuwe tool is bedoeld om COVID-19 te bestrijden, andere ziekten
- IJsbestendige coating voor grote constructies is afhankelijk van een prachtige demonstratie van mechanica

 Wetenschappers creëren een nieuwe elektronegativiteitsschaal
Wetenschappers creëren een nieuwe elektronegativiteitsschaal Familie komt bijeen voor privé-uitzending van astronaut John Glenn
Familie komt bijeen voor privé-uitzending van astronaut John Glenn Hoe herstel je een gebroken hart?
Hoe herstel je een gebroken hart?  Black box onthult laatste momenten van gedoemde Himalaya-klimmers
Black box onthult laatste momenten van gedoemde Himalaya-klimmers De kleur zien van verstrengelde fotonen in moleculaire systemen
De kleur zien van verstrengelde fotonen in moleculaire systemen  De wereld kan waarschijnlijk genoeg koolstofdioxide opvangen en opslaan om de klimaatdoelstellingen te halen
De wereld kan waarschijnlijk genoeg koolstofdioxide opvangen en opslaan om de klimaatdoelstellingen te halen Neutronenstercrash:het geschenk dat zal blijven geven
Neutronenstercrash:het geschenk dat zal blijven geven Coöperatieve jacht vereist minder denkkracht dan eerder werd gedacht
Coöperatieve jacht vereist minder denkkracht dan eerder werd gedacht
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

