
Wetenschap
Hoe Henry Moseley het periodiek systeem herschikte?
In 1913 voerde Moseley een reeks experimenten uit met behulp van röntgenstralen om de verstrooiingspatronen van verschillende elementen te bestuderen. Hij merkte op dat de frequentie van de uitgezonden röntgenstralen op een consistente en voorspelbare manier toenam terwijl hij zich over het periodiek systeem bewoog. Deze waarneming bracht Moseley ertoe te veronderstellen dat het atoomnummer, dat overeenkomt met het aantal protonen in de atoomkern, de fundamentele eigenschap was die de identiteit en positie van een element in het periodiek systeem bepaalde.
Kernpunten van Moseley's herschikking van het periodiek systeem:
Atoomnummer: Moseley stelde het atoomnummer vast als het belangrijkste organiserende principe van het periodiek systeem. Hij toonde aan dat de eigenschappen van elementen nauwer verband hielden met hun atoomnummers dan met hun atoommassa.
Periodieke trends: De periodieke trends van elementen werden duidelijker wanneer ze werden gerangschikt volgens atoomnummers. Elementen met vergelijkbare chemische eigenschappen hadden bijvoorbeeld vaak opeenvolgende atoomnummers.
Gecorrigeerde atoommassa's: Moseley's werk maakte een nauwkeurigere bepaling van de atoommassa's mogelijk, waarbij enkele fouten in eerdere metingen werden gecorrigeerd.
Nieuwe elementen voorspeld: Het periodiek systeem van Moseley voorspelde het bestaan van nieuwe elementen die nog niet ontdekt waren. Hij liet gaten in de tabel achter voor deze ontbrekende elementen, die vervolgens door verdere experimenten werden gevonden en bevestigd.
Overgangsmetalen: De herschikking van Moseley plaatste overgangsmetalen op de juiste posities, waardoor bepaalde afwijkingen in hun eigenschappen en chemisch gedrag in vergelijking met andere elementen werden opgelost.
Impact op de structuur van het periodiek systeem: De herschikking van Moseley resulteerde in een periodiek systeem met elementen gerangschikt in horizontale rijen (punten) en verticale kolommen (groepen). Deze structuur, gebaseerd op atoomnummers, is de moderne opstelling van het periodiek systeem dat tegenwoordig wordt gebruikt.
Concluderend:het werk van Henry Moseley bracht een revolutie teweeg in de organisatie en het begrip van het periodiek systeem. Door het atoomnummer als het fundamentele organiserende principe vast te stellen, bracht Moseley's onderzoek samenhang in de eigenschappen en het gedrag van elementen en maakte het de weg vrij voor verdere vooruitgang in de scheikunde en natuurkunde.
Hoofdlijnen
- G2-fase: wat gebeurt er in deze subfase van de celcyclus?
- Verbetering van de neuronenfabriek - nieuwe modulator van stamcelidentiteit gevonden
- Onderzoek bij wormen biedt een model om te bestuderen hoe het microbioom de ziekte bij mensen beïnvloedt
- Waarom verteert het zoutzuur dat door de maag wordt geproduceerd zijn eigen slijmvliescellen?
- Waarom stak de olifant de weg over? In Maleisië, ze proberen het antwoord te vinden
- Hoe evolueren bacteriën in de darm in de loop van een jaar?
- Hoe reguleren PA-, ABA- en CBF-routes synergetisch de koudetolerantie van meloenen?
- Wat eten we? Onderzoek naar het dieet van dolfijnen
- Hoe dieren te redden door het aantal verkeersslachtoffers te verminderen
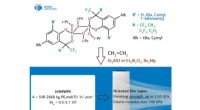
- Een onderzoek naar katalysatoren voor het synthetiseren van polyethyleen met ultrahoog molecuulgewicht
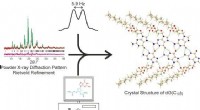
- Nieuwe experimentele strategie verheldert complexe kristalstructuur
- Onderzoekers ontwikkelen een rekrek voor cellen

- Nieuwe lijm kan miljoenen medische procedures veiliger maken, minder invasief voor patiënten

- Wetenschappers ontwikkelen nieuwe theorie van moleculaire evolutie

 Hoe goede darmbacteriën het risico op hartaandoeningen helpen verminderen
Hoe goede darmbacteriën het risico op hartaandoeningen helpen verminderen nieuwe wegen, betere biobrandstoffen
nieuwe wegen, betere biobrandstoffen AI-graanbeoordeling zaait zaden voor een beter rendement
AI-graanbeoordeling zaait zaden voor een beter rendement Sociale media kunnen aandelenrendementen beïnvloeden, professor financiën zegt:
Sociale media kunnen aandelenrendementen beïnvloeden, professor financiën zegt: Cultuur kan verklaren waarom hersenen groter zijn geworden
Cultuur kan verklaren waarom hersenen groter zijn geworden  Wat is de balans tussen zwaartekracht en drijfvermogen?
Wat is de balans tussen zwaartekracht en drijfvermogen?  Hoe een wormgat te herkennen (als ze bestaan)
Hoe een wormgat te herkennen (als ze bestaan) Een student verdunde zorgvuldig 25,0 ml 0,6 M NaOH-oplossing in 475 ml gedestilleerd water. Wat is de molariteitsbase?
Een student verdunde zorgvuldig 25,0 ml 0,6 M NaOH-oplossing in 475 ml gedestilleerd water. Wat is de molariteitsbase?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


