
Wetenschap
Van welke elementengroep is het bekend dat ze een covalente binding hebben?
De groep elementen waarvan het meest bekend is dat ze binden door een covalente binding, is de groep niet-metalen. Niet-metalen zijn elementen die warmte en elektriciteit slecht geleiden en doorgaans een laag smelt- en kookpunt hebben. Niet-metalen zijn doorgaans ook elektronegatiever dan metalen, wat betekent dat ze een grotere aantrekkingskracht hebben op elektronen. Dit elektronegativiteitsverschil tussen niet-metalen zorgt ervoor dat ze elektronen delen om covalente bindingen te vormen. Enkele veel voorkomende voorbeelden van covalente bindingen zijn de bindingen tussen waterstof en zuurstof in water (H2O), de bindingen tussen koolstof en waterstof in methaan (CH4), en de bindingen tussen stikstof en zuurstof in stikstofdioxide (NO2).
 Onderzoek toont aan dat klimaatkoeling invloed heeft op de manier waarop menselijke samenlevingen gedijen of achteruitgaan
Onderzoek toont aan dat klimaatkoeling invloed heeft op de manier waarop menselijke samenlevingen gedijen of achteruitgaan  National Weather Service bevestigt tornado nabij Nashville
National Weather Service bevestigt tornado nabij Nashville Eerder tarwe zaaien kan de opbrengst in India helpen verhogen
Eerder tarwe zaaien kan de opbrengst in India helpen verhogen VS maakt einde aan verbod op nieuwe uraniumwinning in de buurt van Grand Canyon
VS maakt einde aan verbod op nieuwe uraniumwinning in de buurt van Grand Canyon Op dun ijs:nabij de Noordpool, een waarschuwing over klimaatverandering
Op dun ijs:nabij de Noordpool, een waarschuwing over klimaatverandering
Hoofdlijnen
- Mutante cellen die op de een of andere manier geen DNA kunnen kopiëren, blijven zich delen terwijl dat niet zou moeten, met rampzalige gevolgen
- Wat worden clusters van cellichamen genoemd?
- Wetenschappers ontdekken hoe het belangrijkste enzym dat betrokken is bij veroudering, kanker assembleert
- Welke moleculen je op je telefoon achterlaat, onthullen iets over je levensstijl
- Naarmate het klimaat warmer wordt, meer vogelnesten worden vernietigd in Finse landbouwgronden
- Zijn twee fasen van quarantaine beter dan één?
- Hoe staarten gekko's en andere gewervelde dieren helpen grote stappen te maken
- Klimaatverandering kan bamboe-lemuren langzaam uithongeren
- Hoe origami ziektediagnoses kan bepalen
- Natuurlijke antibiotica multi-level aanvalsstrategie voorkomt resistentie
- Een soort mos kan medisch effectiever blijken te zijn dan hennep

- Aanpassingen aan niet-fullereen acceptor voor kleine moleculen in organische dunne film voor zonnecellen verbeteren de efficiëntie

- Onderzoekers printen regenboogkleurstoffen op glinsterende chocolade

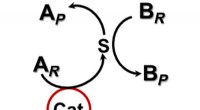
- Chemische reacties versnellen zonder direct contact met een katalysator
 Onderzoek laat zien hoe enzym schade door ultraviolet licht detecteert
Onderzoek laat zien hoe enzym schade door ultraviolet licht detecteert  Hoe kunnen scholen ervoor zorgen dat hoogbegaafde leerlingen de hulp krijgen die ze nodig hebben?
Hoe kunnen scholen ervoor zorgen dat hoogbegaafde leerlingen de hulp krijgen die ze nodig hebben?  Een verbeterde op ruthenium gebaseerde katalysator voor de synthese van primaire amines
Een verbeterde op ruthenium gebaseerde katalysator voor de synthese van primaire amines NIST-team demonstreert hart van atoomklok op chipschaal van de volgende generatie
NIST-team demonstreert hart van atoomklok op chipschaal van de volgende generatie Middeleeuwse literatuur naar het digitale tijdperk brengen
Middeleeuwse literatuur naar het digitale tijdperk brengen Rechter overweegt plan Ryanair om Nederlandse piloten over te dragen
Rechter overweegt plan Ryanair om Nederlandse piloten over te dragen Grafeenspons helpt lithiumzwavelbatterijen nieuw potentieel te bereiken
Grafeenspons helpt lithiumzwavelbatterijen nieuw potentieel te bereiken Statistieken over seksuele intimidatie:onthullen de cijfers de ware omvang van het probleem?
Statistieken over seksuele intimidatie:onthullen de cijfers de ware omvang van het probleem?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

