
Wetenschap
Waarom zijn vloeibare moleculen uit elkaar verwijderd?
In een vloeistof zitten de moleculen niet zo dicht opeengepakt als in een vaste stof, maar ze liggen nog steeds relatief dicht bij elkaar. De intermoleculaire krachten tussen vloeibare moleculen zijn niet sterk genoeg om de moleculen in een vaste positie te houden, maar wel sterk genoeg om te voorkomen dat de moleculen te ver uit elkaar bewegen.
De kinetische energie van vloeibare moleculen is ook hoger dan die van vaste moleculen. Dit betekent dat vloeibare moleculen sneller bewegen en meer botsingen met elkaar hebben. De botsingen tussen vloeibare moleculen helpen voorkomen dat ze samenklonteren en een vaste stof vormen.
De combinatie van intermoleculaire krachten en kinetische energie houdt vloeibare moleculen uit elkaar en zorgt ervoor dat ze gemakkelijk kunnen stromen.
 Microben vormen het toneel voor eerste dieren
Microben vormen het toneel voor eerste dieren Nieuwe stabiele isotopenanalyse stelt de oorsprong van zwarte koolstof in de oceaan in vraag
Nieuwe stabiele isotopenanalyse stelt de oorsprong van zwarte koolstof in de oceaan in vraag Zaterdagcitaten:Tarantula's en hun homies; hoe muggen je vinden; zwarte gaten zijn helemaal niet mysterieus
Zaterdagcitaten:Tarantula's en hun homies; hoe muggen je vinden; zwarte gaten zijn helemaal niet mysterieus  Aanpassingen van een Macaroni-pinguïn
Aanpassingen van een Macaroni-pinguïn  Het verschil tussen menselijke vlooien en hondenvlooien
Het verschil tussen menselijke vlooien en hondenvlooien
Hoofdlijnen
- Verschillen tussen codering en sjabloondraden
- Zooplankton Vs. fytoplankton
- Wat ons zonnebrand bezorgt, beschermt rivierkreeften tegen bacteriën
- Het huwelijk van synthetische biologie en 3D-printen levert programmeerbare levende materialen op
- Wedstrijden om vrouwelijke aandacht maken van mannen betere presteerders - in fruitvliegjes
- Hoe beleid te ontwerpen dat zowel de aquacultuur als de kleinschalige visserij ondersteunt
- Slechts een derde van het gepubliceerde psychologische onderzoek is betrouwbaar – wat nu?
- Vluchtpatronen onthullen hoe muggen gastheren vinden om dodelijke ziekten over te brengen
- Waarom worden sommige aminozuren essentiële aminozuren genoemd?
- Geautomatiseerde chemie zet nieuw tempo voor materiaalontdekking

- Eiwitbatterijen produceren voor veiligere, milieuvriendelijke energieopslag

- Onderzoekers laten kunstmatige haren groeien met slimme natuurkundige truc

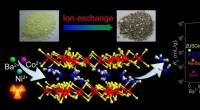
- Selectieve afvang van ionen uit afvalwater met gelaagd metaalsulfide
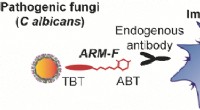
- Neutralisatie van pathogene schimmels met immunotherapeutica met kleine moleculen
 Genderrevolutie in wie de portemonnee vasthoudt
Genderrevolutie in wie de portemonnee vasthoudt Hittegolven stijgen in India naarmate de klimaatverandering intensiveert
Hittegolven stijgen in India naarmate de klimaatverandering intensiveert Math-arrays schrijven
Math-arrays schrijven  Waarom is de diffusiesnelheid in vloeistoffen langzamer dan in gassen?
Waarom is de diffusiesnelheid in vloeistoffen langzamer dan in gassen?  Opgravingen tonen aan dat het afgelegen Griekse eilandje een vroeg industrieel centrum was
Opgravingen tonen aan dat het afgelegen Griekse eilandje een vroeg industrieel centrum was  Afbeelding:Barchan en lineaire duinen op Mars
Afbeelding:Barchan en lineaire duinen op Mars  Hoe verschuivende wolkenpatronen de klimaatverandering verergeren
Hoe verschuivende wolkenpatronen de klimaatverandering verergeren  Nieuwe symmetriedoorbrekende methode opent weg voor bioactieve stoffen
Nieuwe symmetriedoorbrekende methode opent weg voor bioactieve stoffen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

