
Wetenschap
Er is een volume van 31,43 ml 0,108 M NaOH nodig om het fenolftaleïne-eindpunt te bereiken bij titratie. Een monsterazijn van 4,441 g. Bereken het percentage azijnzuurazijn?
Stap 1:Bereken het aantal mol NaOH dat bij de titratie is gebruikt
Mol NaOH =concentratie NaOH x volume gebruikt NaOH
Mol NaOH =0,108 M × 31,43 ml / 1000 ml/l
Mol NaOH =0,0033846 mol
Stap 2:Bepaal het aantal mol azijnzuur
Omdat de reactie tussen NaOH en azijnzuur een stoichiometrie van 1:1 is, zijn de aantallen molen azijnzuur gelijk aan de molen NaOH die bij de titratie worden gebruikt.
Mol azijnzuur =0,0033846 mol
Stap 3:Bereken de massa azijnzuur
Molaire massa azijnzuur (CH3COOH) =60,05 g/mol
Massa azijnzuur =Mol azijnzuur × Molaire massa azijnzuur
Massa azijnzuur =0,0033846 mol × 60,05 g/mol
Massa azijnzuur =0,2031 gram
Stap 4:Bereken het percentage azijnzuur in azijn
Percentage azijnzuur =(massa azijnzuur / massa azijn) × 100%
Percentage azijnzuur =(0,2031 g / 4,441 g) × 100%
Percentage azijnzuur =4,572%
Daarom bevat het azijnmonster 4,572% azijnzuur.
 Vermindering van houtverbranding door plattelandsmensen in China leidt tot minder vervuiling door fijnstof
Vermindering van houtverbranding door plattelandsmensen in China leidt tot minder vervuiling door fijnstof De grootste steden van Zuid-Afrika zitten zonder water, maar de dammen zijn vol:wat is er misgegaan?
De grootste steden van Zuid-Afrika zitten zonder water, maar de dammen zijn vol:wat is er misgegaan?  De overheid heeft een nieuw rapport over klimaatverandering en (Spoiler Alert) vrijgegeven. Het is echt slecht
De overheid heeft een nieuw rapport over klimaatverandering en (Spoiler Alert) vrijgegeven. Het is echt slecht  Groenere en beter beloopbare stedelijke gebieden moedigen fysieke activiteit aan
Groenere en beter beloopbare stedelijke gebieden moedigen fysieke activiteit aan Klimaatverandering maakt bouwen, visserij en andere gevaarlijke industrieën nog riskanter
Klimaatverandering maakt bouwen, visserij en andere gevaarlijke industrieën nog riskanter
Hoofdlijnen
- Vreemde wereld van Australische bijen:hoe één soort genderevenwicht in het nest creëert
- UITLEG:Wat zijn krekels en waarom irriteren ze sommige mensen?
- Wat zou er met een eiwit gebeuren als het gen van DNA zou worden veranderd?
- Om de effecten van langere, hetere zomers te bestuderen, slepen ecologen 5000 kilo zand de berg op
- Boomwoning, kokosnootkrakende gigantische rat ontdekt op de Salomonseilanden
- Waarom banken hun buitenlandse activa niet voldoende diversifiëren
- Depolarisatie en repolarisatie van het celmembraan
- Hoe belangrijke genen samenwerken om een gezonde huid te maken
- Eilandvogels zijn flexibeler dan eerder werd gedacht
- Biomarkers die kunnen helpen bepalen wie risico loopt op ernstige COVID-19-symptomen

- Wetenschappers maken onderdelen van titanium met behulp van additieve technologieën

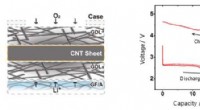
- Ontwikkeling van lithium-luchtbatterijen met ultrahoge capaciteit met behulp van CNT-blad-luchtelektroden
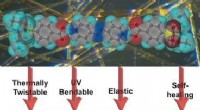
- Organische kristallen draaien, kromming, en genees
- Samenstellingsontwerp van legeringen met meerdere componenten door screening met hoge doorvoer

 Hoe te beslissen hoe te stemmen - advies van een psycholoog
Hoe te beslissen hoe te stemmen - advies van een psycholoog  Elektronisch oog:technologie voor storingspreventie
Elektronisch oog:technologie voor storingspreventie SpaceX Starship-rakettest eindigt in een nieuwe mislukking:Musk
SpaceX Starship-rakettest eindigt in een nieuwe mislukking:Musk NASA-schadekaart helpt bij natuurbranden in Californië
NASA-schadekaart helpt bij natuurbranden in Californië Chemici volgen moleculen in nanowells, volg katalytische reacties in nano-opsluiting
Chemici volgen moleculen in nanowells, volg katalytische reacties in nano-opsluiting De kunst van moleculair tapijtweven:2D-netwerken van boorzuren
De kunst van moleculair tapijtweven:2D-netwerken van boorzuren Kan het omkeren van de opwarming van de aarde een ijstijd inluiden?
Kan het omkeren van de opwarming van de aarde een ijstijd inluiden?  Mojo Vision pronkt met displaytechnologie voor augmented reality
Mojo Vision pronkt met displaytechnologie voor augmented reality
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

