
Wetenschap
Welke indicator kun je kiezen voor de titratie van oxaalzuur met natriumhydroxide?
Hier is de uitleg:
Zuur-base-reactie:
Oxaalzuur (H2C2O4) is een diprotisch zuur, wat betekent dat het twee protonen (H+) per molecuul kan doneren. Natriumhydroxide (NaOH) is een sterke base die volledig dissocieert in water, waarbij hydroxide-ionen (OH-) vrijkomen. De reactie tussen oxaalzuur en natriumhydroxide kan als volgt worden weergegeven:
H2C2O4 + 2NaOH → Na2C2O4 + 2H2O
Equivalentiepunt:
Het equivalentiepunt bij titratie wordt bereikt wanneer het aantal mol zuur en base stoichiometrisch gelijk zijn. In het geval van oxaalzuur en natriumhydroxide wordt het equivalentiepunt bereikt wanneer alle oxaalzuurmoleculen hebben gereageerd met een gelijk aantal hydroxide-ionen. Op dit punt is de oplossing neutraal, wat betekent dat deze geen zure of basische pH heeft.
Fenolftaleïne als indicator:
Fenolftaleïne is een veelgebruikte zuur-base-indicator die een kleurverandering ondergaat in het pH-bereik van ongeveer 8,3 tot 10,0. In zijn zure vorm is fenolftaleïne kleurloos en wanneer de pH boven de 8,3 komt, wordt het roze.
Bij de titratie van oxaalzuur met natriumhydroxide kan fenolftaleïne effectief het equivalentiepunt aangeven. Als u tijdens de titratie natriumhydroxide aan de oxaalzuuroplossing toevoegt, neemt de pH geleidelijk toe. Aanvankelijk zal de oplossing zuur zijn en zal de fenolftaleïne-indicator kleurloos blijven. Naarmate de pH het equivalentiepunt nadert, wordt de oplossing echter minder zuur en bereikt uiteindelijk de neutraliteit (pH ≈ 7). Op dit punt zal de toevoeging van zelfs een kleine hoeveelheid overmaat natriumhydroxide een aanzienlijke pH-verhoging veroorzaken vanwege de sterke basiciteit van NaOH. Deze plotselinge pH-verandering zorgt ervoor dat de fenolftaleïne-indicator roze kleurt.
Daarom geeft het verschijnen van een aanhoudende roze kleur in de oplossing aan dat het equivalentiepunt is bereikt, wat de voltooiing van de titratie aangeeft. De kleurverandering van fenolftaleïne in het pH-bereik dichtbij neutraliteit maakt het een geschikte indicator voor titraties waarbij zwakke zuren zoals oxaalzuur en sterke basen zoals natriumhydroxide betrokken zijn.
 Pulsen van een atoomscherpe punt stellen onderzoekers in staat om naar believen chemische bindingen te verbreken en te vormen
Pulsen van een atoomscherpe punt stellen onderzoekers in staat om naar believen chemische bindingen te verbreken en te vormen Nieuwe studie identificeert mogelijke voorouders van RNA
Nieuwe studie identificeert mogelijke voorouders van RNA Waarom reist ammoniak sneller dan zoutzuur?
Waarom reist ammoniak sneller dan zoutzuur?  Betekent ontbinding hetzelfde als synthese?
Betekent ontbinding hetzelfde als synthese?  Team krijgt inzicht in de oxidelaag van roestvrij staal
Team krijgt inzicht in de oxidelaag van roestvrij staal
 Bosbrandrook is slecht voor je ogen, ook - hier kun je ze beschermen
Bosbrandrook is slecht voor je ogen, ook - hier kun je ze beschermen Braziliaanse rechtbank schorst decreet dat mijnbouw in Amazone-reserves toestaat
Braziliaanse rechtbank schorst decreet dat mijnbouw in Amazone-reserves toestaat Nieuwe analyse ziet een piek in het mondiale zeeniveau in 2023 als gevolg van El Niño
Nieuwe analyse ziet een piek in het mondiale zeeniveau in 2023 als gevolg van El Niño  2020 was een verschrikkelijk jaar voor klimaatrampen, maar er zijn redenen voor hoop in 2021
2020 was een verschrikkelijk jaar voor klimaatrampen, maar er zijn redenen voor hoop in 2021 Verandering in landgebruik leidt tot meer overstromingen in Indonesië, studie toont
Verandering in landgebruik leidt tot meer overstromingen in Indonesië, studie toont
Hoofdlijnen
- Wetenschappers onthullen hoe een weinig bekende amoebe een bacterie overspoelde om fotosynthetisch te worden
- Ze aanzetten, uitzetten – hoe je stamcellen onder controle kunt houden
- Vergelijk en vergelijk DNA & RNA
- Wilt u kakkerlakkenseks verminderen? Blokkeer een enzym
- Muizensperma overleeft in de ruimte, maar kunnen menselijke baby's dat ook?
- Wat zijn drie dingen die bepalen of een molecuul in een celmembraan kan diffunderen?
- Wat is een lichaamsbuis in een microscoop?
- Red Tit-toxine stuurde hen naar het ziekenhuis. Kijk wat er gebeurde met een paar Florida-schildpadden
- Ontdekking van nieuwe microscopisch kleine soorten vergroot de levensboom
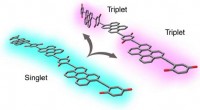
- Twee-voor-één energie van fotonen, nu beter dan ooit
- Een thermometer die kan worden uitgerekt en vervormd door water
- Nieuw lichtgewicht metaal zo vormbaar als aluminium plaatwerk met 1,5 keer hogere sterkte

- Betere adsorptie van chemomedicijnen op gerichte toedieningscapsules

- Video:Waarom ruikt de maan naar buskruit?

 Hoe ontploft vuurwerk in specifieke vormen?
Hoe ontploft vuurwerk in specifieke vormen?  Welke elementen zitten in kaliumhydroxide?
Welke elementen zitten in kaliumhydroxide?  Waarom probeert technologiegigant Apple onze leraren les te geven?
Waarom probeert technologiegigant Apple onze leraren les te geven? Waarom de autoverkoop sterk is in de VS (update)
Waarom de autoverkoop sterk is in de VS (update)  De Hitomi-satelliet gaf een korte glimp van het heelal,
De Hitomi-satelliet gaf een korte glimp van het heelal,  Ruimteweer voorspellen is moeilijk, maar een nieuwe Australische satelliet zou het makkelijker kunnen maken
Ruimteweer voorspellen is moeilijk, maar een nieuwe Australische satelliet zou het makkelijker kunnen maken Hoe maak je een voedselweb-diagram
Hoe maak je een voedselweb-diagram Verstoringen van de relatie tussen verkoper en klant. Is dat altijd erg?
Verstoringen van de relatie tussen verkoper en klant. Is dat altijd erg?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

