
Wetenschap
Hoeveel mol zuurstofgas is nodig om te reageren met 4,0 Mg?
Om het aantal mol zuurstofgas te berekenen dat nodig is om te reageren met 4,0 g Mg, moeten we rekening houden met de uitgebalanceerde chemische vergelijking voor de verbranding van magnesium:
$$2Mg(s) + O_2(g) → 2MgO(s)$$
Deze vergelijking vertelt ons dat 2 mol Mg reageren met 1 mol O2. Eerst moeten we de gegeven massa van Mg (4,0 g) omzetten in mol met behulp van de molaire massa (24,305 g/mol):
$$4.0\text{ g Mg} \times \frac{1\text{ mol Mg}}{24.305\text{ g Mg}} =0,164\text{ mol Mg}$$
Volgens de uitgebalanceerde chemische vergelijking is voor elke 2 mol Mg 1 mol O2 nodig. Daarom is het aantal mol zuurstofgas dat nodig is om te reageren met 0,164 mol Mg:
$$0,164\text{ mol Mg} \times \frac{1\text{ mol O}_2}{2\text{ mol Mg}} =0,082\text{ mol O}_2$$
Er zijn dus 0,082 mol zuurstofgas nodig om te reageren met 4,0 g Mg.
 Zijn peptidebindingen sterk of zwak?
Zijn peptidebindingen sterk of zwak?  Synthetische brandstoffen kunnen de ecologische voetafdruk verkleinen
Synthetische brandstoffen kunnen de ecologische voetafdruk verkleinen Moleculaire steiger voor het wijzigen van fluorescerende verbindingen die worden gebruikt in biologische beeldvorming
Moleculaire steiger voor het wijzigen van fluorescerende verbindingen die worden gebruikt in biologische beeldvorming Ontwikkelen van een breed temperatuurbereik en hoogspannings waterige MXene planaire micro-supercondensatoren
Ontwikkelen van een breed temperatuurbereik en hoogspannings waterige MXene planaire micro-supercondensatoren Metaalfluisteren:een betere manier vinden om edele metalen uit elektronisch afval te halen
Metaalfluisteren:een betere manier vinden om edele metalen uit elektronisch afval te halen
 NASA-NOAA-satelliet analyseert tyfoon Wutip
NASA-NOAA-satelliet analyseert tyfoon Wutip Overstromingen in Ghana doden 34 bij zware regenval
Overstromingen in Ghana doden 34 bij zware regenval Wat is déjà vu?
Wat is déjà vu?  Door de opwarming van de aarde zullen ecosystemen meer methaan produceren dan eerst werd voorspeld
Door de opwarming van de aarde zullen ecosystemen meer methaan produceren dan eerst werd voorspeld Afvalmelk kan worden gebruikt om de uitstoot van kooldioxide in elektriciteitscentrales te verminderen
Afvalmelk kan worden gebruikt om de uitstoot van kooldioxide in elektriciteitscentrales te verminderen
Hoofdlijnen
- Wetenschappers onthullen de ware identiteit van een Chinese octopus
- De structuur van een eukaryote cel
- Beschrijving van de basisfuncties van enzymen in cellen
- Hoe maak je een celmodel van een Amoeba
- Wetenschappers geven 's werelds eerste DNA-kaart van een bedreigde Australische muis vrij, en het zal helpen om deze te redden
- Nieuwe AI-tool legt vast hoe eiwitten zich in context gedragen
- Geluid onthult dat gigantische blauwe vinvissen met de wind dansen om voedsel te vinden
- Hoe deep learning de analyse van celbeelden mogelijk maakt
- Biologen leggen uit hoe organismen mutaties kunnen tolereren en zich toch kunnen aanpassen aan veranderingen in het milieu
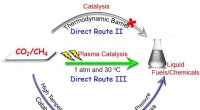
- Doorbraak in directe activering van CO2 en CH4 tot vloeibare brandstoffen en chemicaliën
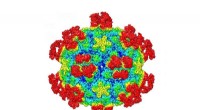
- Nieuw mechanisme om virussen te vernietigen kan leiden tot toekomstige therapieën
- Onderzoeksteam helpt Arcteryx groen en droog te blijven met waterafstotende stoffen van de volgende generatie

- Onder verschillende omstandigheden onderzoeken hoe oppervlakken veranderen in contact met reactieve gasfasen
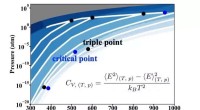
- Studie suggereert route naar verbetering oplaadbare lithiumbatterijen

 Titaanatoom dat op twee plaatsen tegelijk in kristal bestaat en de oorzaak is van een ongewoon fenomeen
Titaanatoom dat op twee plaatsen tegelijk in kristal bestaat en de oorzaak is van een ongewoon fenomeen Waarom de meeste economen lockdowns blijven steunen
Waarom de meeste economen lockdowns blijven steunen Vraag ons of het volgende waar is over middelpuntzoekende kracht?
Vraag ons of het volgende waar is over middelpuntzoekende kracht?  Hoeveel covalente bindingen verbinden de atomen in een ammoniakmolecuul (NH3)?
Hoeveel covalente bindingen verbinden de atomen in een ammoniakmolecuul (NH3)?  Hoe Giraffes Mate?
Hoe Giraffes Mate?  Onderzoekers ontwikkelen nieuwe toolkit voor actie op het gebied van sociale rechtvaardigheid
Onderzoekers ontwikkelen nieuwe toolkit voor actie op het gebied van sociale rechtvaardigheid Nieuwe CEO van Nissan brengt wereldwijde vooruitzichten, maar staat voor een zware taak
Nieuwe CEO van Nissan brengt wereldwijde vooruitzichten, maar staat voor een zware taak Kan pizzakruid winterbraakziekte voorkomen?
Kan pizzakruid winterbraakziekte voorkomen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

