
Wetenschap
Hoeveel equivalente Lewis-structuren zijn er nodig om de binding in SF4O te beschrijven?
Er zijn twee equivalente Lewis-structuren nodig om de binding in SF4O te beschrijven. Beide structuren omvatten de binding van één zwavelatoom aan drie fluoratomen en aan drie zuurstofatomen tetraëdrisch. In één tekening verbinden dubbele bindingen zwavel met één zuurstof en één fluor; in de tweede is een van de zuurstofbindingen met zwavel een meervoudige binding. Deze meervoudige bindingen kunnen echter snel terugkeren van het ene zuurstofatoom naar het andere, waardoor een symmetrische ladingsverdeling over alle vier de O-atomen ontstaat, waardoor deze twee structuren gelijkwaardig worden:
\[:\ddot{\text{O}}-\text{S}(=\text{F})_{2}(\text{=O})_{2} \rightleftharpoons :\ddot{\text {O}}=\text{S}(=\text{F})_{2}(\text{=O})\text{O}^-\]
 Hoeveel mol KNO3 moet in totaal in water worden opgelost om van 1,5 liter een stroom van 2,0 M te maken?
Hoeveel mol KNO3 moet in totaal in water worden opgelost om van 1,5 liter een stroom van 2,0 M te maken?  Carbonitride-aerogels bemiddelen de fotokatalytische omzetting van water
Carbonitride-aerogels bemiddelen de fotokatalytische omzetting van water Laserstraalexcitatie heeft geen invloed op de nucleofiele substitutiereactie
Laserstraalexcitatie heeft geen invloed op de nucleofiele substitutiereactie Onderzoekers ontwikkelen een koolstofveer met hoge samendrukbaarheid en rekbaarheid
Onderzoekers ontwikkelen een koolstofveer met hoge samendrukbaarheid en rekbaarheid Is CH4 een convalente of ionische binding?
Is CH4 een convalente of ionische binding?
 Patronen in permafrostbodems kunnen modellen voor klimaatverandering helpen
Patronen in permafrostbodems kunnen modellen voor klimaatverandering helpen Hoe zit het met de recente wilde tornado's? Deskundige weegt mee
Hoe zit het met de recente wilde tornado's? Deskundige weegt mee  Studie onderzoekt hoe gematigde regenwouden de strijd tegen klimaatverandering kunnen ondersteunen
Studie onderzoekt hoe gematigde regenwouden de strijd tegen klimaatverandering kunnen ondersteunen  Een effectieve oplossing voor klimaatverandering kan in rotsen onder onze voeten liggen
Een effectieve oplossing voor klimaatverandering kan in rotsen onder onze voeten liggen Hoe beïnvloeden brandemissies van industriële plantages de luchtkwaliteit in de Equatoriale ZEE?
Hoe beïnvloeden brandemissies van industriële plantages de luchtkwaliteit in de Equatoriale ZEE?
Hoofdlijnen
- Onderzoek verduidelijkt de functie van de nucleaire hormoonreceptor in planten
- Waarom is de trekduif uitgestorven?
- Opkomende infectieziekte bedreigt Darwins kikker met uitsterven
- De loonkloof in de wetenschap:genderdiscriminatie?
- Wat is het verschil tussen sporenmakers en zaadmakers?
- Zal klimaatverandering het risico op aflatoxine in Amerikaanse maïs vergroten?
- Er zijn nieuwe details onthuld over hoe planten een optimale sperma-ei-verhouding behouden
- Wat zijn C2-planten?
- Diverse landschappen in het hart van bijenbescherming
- Nieuwe katalysator bewezen efficiënt in elektrosynthese van ammoniak

- Nieuwe aanpak creëert een uitzonderlijke katalysator met één atoom voor watersplitsing

- Hoe werkt vuurwerk? Een pyrotechnisch scheikundige legt de wetenschap uit achter de schitterende kleuren en geluiden

- Ontdekking kan leiden tot nieuw katalysatorontwerp om stikstofoxiden in dieseluitlaatgassen te verminderen

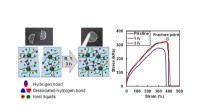
- De toekomst van elektronische apparaten:sterke en zelfherstellende iongels
 Een model van een pandas maken Habitat
Een model van een pandas maken Habitat Thermodynamische magie maakt koeling mogelijk zonder energieverbruik
Thermodynamische magie maakt koeling mogelijk zonder energieverbruik Storm teistert Caribisch gebied met harde wind, regen op weg naar de VS
Storm teistert Caribisch gebied met harde wind, regen op weg naar de VS Oceanen veranderen van vriend in vijand, waarschuwt historisch VN-klimaatrapport
Oceanen veranderen van vriend in vijand, waarschuwt historisch VN-klimaatrapport Waar gaat houtskool, of zwarte koolstof, in de bodem naartoe?
Waar gaat houtskool, of zwarte koolstof, in de bodem naartoe?  Onderzoekers ontwikkelen technologie waarmee standaardcamera's hyperspectrale beelden kunnen produceren
Onderzoekers ontwikkelen technologie waarmee standaardcamera's hyperspectrale beelden kunnen produceren Overstappen op e-auto's kost Duitsland 75,- 000 banen:studeren
Overstappen op e-auto's kost Duitsland 75,- 000 banen:studeren Wat als we geen maan hadden?
Wat als we geen maan hadden?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

